题目内容
6.既能与酸又能与碱反应是两性化合物的特征.下列物质属于两性化合物的是( )| A. | A1 | B. | Na2CO3 | C. | A1(OH)3 | D. | (NH4)2SO4 |
分析 性物质指即能与酸反应,又能与碱作用生成盐和水的化合物,如Al2O3、ZnO、Zn(OH)2、Al(OH)3、氨基酸、蛋白质等,据此解答.
解答 解:A.铝是单质,不是化合物,故A不选;
B.碳酸钠与碱不反应,故B不选;
C.氢氧化铝与盐酸、氢氧化钠溶液都反应,且生成产物都是盐和水,符合两性物质的概念,属于两性化合物,故C选;
D.硫酸铵与盐酸不反应,不符合两性物质的概念,不是两性物质,故D不选;
故选:C.
点评 本题考查了两性物质的判断,准确把握两性物质的概念是解题关键,注意既能与酸反应又能与碱反应的物质不一定是两性物质,两性物质一定既能与酸反应又能与碱反应,题目难度不大.

练习册系列答案
 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
14.下列有关元素周期律的叙述中,正确的是( )
| A. | 非金属性强弱:F2<Cl2 | B. | 金属性强弱:K<Na | ||
| C. | 酸性强弱:H2SO4<HClO4 | D. | 碱性强弱:NaOH<Mg(OH)2 |
1.下列单质氧化性最强的是( )
| A. | F2 | B. | Cl2 | C. | Br2 | D. | I2 |
11.现有8种元素的性质、数据如下表所列,它们属于第二或第三周期.
回答下列问题:
(1)③的元素符号是Li,⑧的元素名称是硼.
(2)在最高价氧化物的水化物中,酸性最强的化合物的名称是高氯酸.
碱性最强的化合物的电子式是: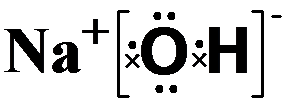 ,属离子化合物(填“离子”或“共价”).
,属离子化合物(填“离子”或“共价”).
(3)比较④和⑦的氢化物的稳定性(用分子式表示)NH3>PH3.
(4)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:NH3+HNO3=NH4NO3.
(5)写出②最高价氧化物对应水化物跟⑤的氢化物水溶液反应的离子方程式:Mg(OH)2+2H+=Mg2++2H2O.
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(1)③的元素符号是Li,⑧的元素名称是硼.
(2)在最高价氧化物的水化物中,酸性最强的化合物的名称是高氯酸.
碱性最强的化合物的电子式是:
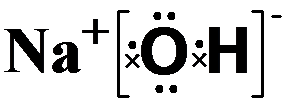 ,属离子化合物(填“离子”或“共价”).
,属离子化合物(填“离子”或“共价”).(3)比较④和⑦的氢化物的稳定性(用分子式表示)NH3>PH3.
(4)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:NH3+HNO3=NH4NO3.
(5)写出②最高价氧化物对应水化物跟⑤的氢化物水溶液反应的离子方程式:Mg(OH)2+2H+=Mg2++2H2O.
18.向明矾溶液中逐滴加入Ba(OH)2溶液,当SO42-全部沉淀时,铝元素的主要存在形式为( )
| A. | AlO2- | B. | Al3+ | C. | Al(OH)3 | D. | Al(OH)3和Al3+ |
15.下列说法错误的是( )
| A. | 同浓度的下列溶液,c(NH4+)大小顺序:(NH4)2SO4>NH4HSO4>NH4Cl>NH4HCO3 | |
| B. | 同浓度的下列溶液,pH值大小顺序:Na2CO3>NaClO>NaHCO3>CH3COONa | |
| C. | 用水冲洗BaSO4比用稀硫酸冲洗损失大 | |
| D. | 用惰性电极电解某溶液,两极分别产生H2和O2,pH值一定升高 |
16.对下列装置图的叙述正确的是( )


| A. | 装置①可用于加热蒸干氯化铵溶液得到氯化铵晶体 | |
| B. | 装置②可用于铜和稀硝酸制取并收集少量NO | |
| C. | 装置③可用于证明铁生锈氧气参与反应 | |
| D. | 苯萃取碘水中的碘后,从装置④下口放出的是碘的苯溶液 |