题目内容
Ⅰ.中学课本中介绍了如下实验:把一端弯成螺旋状的铜丝放在酒精灯外焰加热,待铜丝表面变黑后立即把它插入盛有约2mL乙醇的试管里,反复操作几次.请你评价若用上述方法制取乙醛存在哪些不足(写出两点).
Ⅱ.某课外活动小组利用下图装置进行乙醇的催化氧化实验并制取乙醛,图中铁架台等装置已略去,粗黑线表示乳胶管.请填写下列空白:

(1)实验时,先加热玻璃管乙中的镀银铜丝,约1分钟后鼓入空气,此时铜丝即呈红热状态.若把酒精灯撤走,控制一定的鼓气速度,铜丝能长时间保持红热直到实验结束.
①乙醇的催化氧化反应是 反应(“放热”或“吸热”),该反应的化学方程式为 .
②控制鼓气速度的方法主要看 ,若鼓气速度过快则会 ,若鼓气速度过慢则会 .
(2)若试管丁中用水吸收产物,则要在导管乙、丙之间接上戊装置,其连接方法是(填戊装置中导管代号):乙接 、 接丙.
Ⅱ.某课外活动小组利用下图装置进行乙醇的催化氧化实验并制取乙醛,图中铁架台等装置已略去,粗黑线表示乳胶管.请填写下列空白:

(1)实验时,先加热玻璃管乙中的镀银铜丝,约1分钟后鼓入空气,此时铜丝即呈红热状态.若把酒精灯撤走,控制一定的鼓气速度,铜丝能长时间保持红热直到实验结束.
①乙醇的催化氧化反应是
②控制鼓气速度的方法主要看
(2)若试管丁中用水吸收产物,则要在导管乙、丙之间接上戊装置,其连接方法是(填戊装置中导管代号):乙接
考点:乙醇的催化氧化实验
专题:实验题
分析:Ⅰ.结合题干描述内容,从实验操作是否简便、乙醇的转化率大小进行分析;
Ⅱ.(1)①该反应引发后,不需加热即可进行,说明反应是放热的;乙醇催化氧化生成乙醛和水,据此写出反应的化学方程式;
②根据甲中单位时间内的气泡数来控制气流;若鼓气速度过快,带走过多热量,难以保证反应所需温度;若鼓气速度过慢,催化氧化反应放热太少,达不到反应所需温度反应停止;
(2)安全瓶中的导管是“短进长出”的方式,即b管进入,a管导出.
Ⅱ.(1)①该反应引发后,不需加热即可进行,说明反应是放热的;乙醇催化氧化生成乙醛和水,据此写出反应的化学方程式;
②根据甲中单位时间内的气泡数来控制气流;若鼓气速度过快,带走过多热量,难以保证反应所需温度;若鼓气速度过慢,催化氧化反应放热太少,达不到反应所需温度反应停止;
(2)安全瓶中的导管是“短进长出”的方式,即b管进入,a管导出.
解答:
解:Ⅰ.根据题干描述内容可知,该实验操作存在的不足为:实验操作比较麻烦,且乙醇的转化率较低,
故答案为:操作麻烦、乙醇转化率低;
Ⅱ.(1)①实验时,先加热玻璃管乙中的镀银钢丝,约1分钟后鼓入空气,此时铜丝即呈红热状态,若把酒精灯撤走,控制一定的鼓气速度,铜丝能长时间保持红热直到实验结束,说明反应引发后,不需加热即可进行到底,证明该反应是放热的反应;
乙醇发生催化氧化生成乙醛和水,反应的化学方程式为:2CH3CH2OH+O2
2CH3CHO+H2O,
故答案为:放热;2CH3CH2OH+O2
2CH3CHO+H2O;
②甲中单位时间内的气泡数越多,气流速度越大,反之越小,可以根据甲中单位时间内的气泡数来控制气流;
若鼓气速度过快则会因气流过大,带走过多热量,难以保证反应所需温度,导致反应停止;
若鼓气速度过慢,导致催化氧化反应放热太少,达不到反应所需温度,反应停止;
故答案为:控制甲中单位时间内气泡数;带走过多热量,难以保证反应所需温度;反应放热太少,不能达到反应所需温度;
(2)为防止防止丁中水倒吸,安全瓶中的导气管是“短进长出”,所以乙接b,a接,
故答案为:b;a.
故答案为:操作麻烦、乙醇转化率低;
Ⅱ.(1)①实验时,先加热玻璃管乙中的镀银钢丝,约1分钟后鼓入空气,此时铜丝即呈红热状态,若把酒精灯撤走,控制一定的鼓气速度,铜丝能长时间保持红热直到实验结束,说明反应引发后,不需加热即可进行到底,证明该反应是放热的反应;
乙醇发生催化氧化生成乙醛和水,反应的化学方程式为:2CH3CH2OH+O2
| Cu |
| △ |
故答案为:放热;2CH3CH2OH+O2
| Cu |
| △ |
②甲中单位时间内的气泡数越多,气流速度越大,反之越小,可以根据甲中单位时间内的气泡数来控制气流;
若鼓气速度过快则会因气流过大,带走过多热量,难以保证反应所需温度,导致反应停止;
若鼓气速度过慢,导致催化氧化反应放热太少,达不到反应所需温度,反应停止;
故答案为:控制甲中单位时间内气泡数;带走过多热量,难以保证反应所需温度;反应放热太少,不能达到反应所需温度;
(2)为防止防止丁中水倒吸,安全瓶中的导气管是“短进长出”,所以乙接b,a接,
故答案为:b;a.
点评:本题考查了乙醇的催化氧化实验,题目难度中等,注意掌握乙醇的化学性质,明确乙醇的催化氧化实验原理及操作方法是解答本题的关键,试题培养了学生的分析、理解能力及化学实验能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
设NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A、1 mol Na2O2跟 H2O反应转移电子的数目为2NA |
| B、1 mol氯气跟NaOH反应转移电子的数目为NA |
| C、常温常压下,22.4 L氯气所含原子数为2NA |
| D、标准状况下,22.4 L蒸馏水所含分子数为NA |
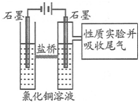 利用如图装置作电解50mL 0.5mol/L的CuCl2溶液实验.
利用如图装置作电解50mL 0.5mol/L的CuCl2溶液实验. 的系统命名是:
的系统命名是: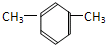 的名称是
的名称是 的系统命名是
的系统命名是