题目内容
4.设NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 2.0gH218O与D20的混合物中所含中子数为NA | |
| B. | 等物质的量的水与重水含有的中子数相等 | |
| C. | 18gD20和18gH20中含有的质子数均为10NA | |
| D. | 235g核素$\left.\begin{array}{l}{235}\\{92}\end{array}\right.$U发生裂变反应:$\left.\begin{array}{l}{235}\\{92}\end{array}\right.$U+$\left.\begin{array}{l}{1}\\{0}\end{array}\right.$n$\frac{\underline{\;裂变\;}}{\;}$$\left.\begin{array}{l}{90}\\{38}\end{array}\right.$Sr+$\left.\begin{array}{l}{136}\\{54}\end{array}\right.$U+10$\left.\begin{array}{l}{1}\\{0}\end{array}\right.$n净产生的中子($\left.\begin{array}{l}{1}\\{0}\end{array}\right.$n)数为10NA |
分析 A.H218O与D2O的摩尔质量均为20g/mol,且H218O与D2O中均含10个中子;
B.H和D原子的中子数不同;
C.D20和18gH20的摩尔质量分别为20g/mol和18g/mol;
D.92235U+01n$\frac{\underline{\;裂变\;}}{\;}$3890Sr+54136U+1001n净产生的中子为10-1=9个.
解答 解:A.H218O与D2O的摩尔质量均为20g/mol,故2.0g混合物的物质的量为0.1mol,而且H218O与D2O中均含10个中子,故0.1mol混合物中含1mol中子即NA个,故A正确;
B.物质的量相等的H2O与D2O含有的中子数比值为(8):(8+2×1)=8:10,中子数不同,故B错误;
C.18gD20和18gH20物质的量分别为0.9mol和1mol,含有的质子数分别为9NA和10NA,故C错误;
D.92235U+01n$\frac{\underline{\;裂变\;}}{\;}$3890Sr+54136U+1001n净产生的中子为10-1=9个,则235g核素92235U发生裂变反应净产生的中子(01n)数为9NA,故D错误;
故选:D.
点评 本题考查了阿伏伽德罗常数及计算,为高频考点,侧重于物质的结构的考查,明确原子结构是解题关键,题目难度中等.

练习册系列答案
 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案
相关题目
15.将蔗糖水解,并用新制的氢氧化铜悬浊液检验其水解产物的实验中,要进行的主要操作是( )
①加热
②滴入稀硫酸
③加入新制的氢氧化铜悬浊液
④加入适量的氢氧化钠溶液调节至碱性.
①加热
②滴入稀硫酸
③加入新制的氢氧化铜悬浊液
④加入适量的氢氧化钠溶液调节至碱性.
| A. | ①→②→③→④→① | B. | ②→①→④→③→① | C. | ②→④→①→③→① | D. | ③→④→①→②→① |
19.下列各组有机物中,互为同分异构体的是( )
| A. |  | B. | 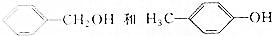 | ||
| C. |  | D. | 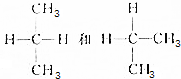 |
9.将一定量的钠铝合金置于水中,合金全部溶解,得到20mL c(OH-)=1mol/L的溶液,然后向溶液中滴加l mol•L-1的盐酸至沉淀质量最大时,消耗盐酸40mL,原合金中钠的质量为( )
| A. | 0.46g | B. | 0.69g | C. | 0.92g | D. | 0.23g |
6.下列物质不属于既能跟盐酸反应又能跟NaOH溶液反应的是( )
| A. | Al | B. | Al2O3 | C. | Na2CO3 | D. | NaHCO3 |
3.现有25mL2mol•L-1的Na2CO3溶液和75mL1mol•L-1的稀盐酸.①将Na2CO3溶液缓慢滴到稀盐酸中;②将稀盐酸缓缓滴到Na2CO3溶液中,在标准状况下产生气体的体积情况是( )
| A. | 均为0.56 L | B. | ①=② | C. | ①>② | D. | ②>① |

 .
.