题目内容
某同学为进行中和热测定实验,已知实验室有0.50mol/LHCl溶液和NaOH固体及其他必要的试剂和仪器.
该同学先配制0.55mol/L的NaOH溶液并测定其准确浓度.其操作步骤如下:A、在250mL的容量瓶中定容配成250mL烧碱溶液;B、用移液管移取25mL烧碱溶液于锥形瓶中并滴加几滴甲基橙指示剂;C、在天平上准确称取烧碱样品5.5g,在烧杯中加蒸馏水溶解;D、将标准盐酸溶液装入酸式滴定管,调整液面,并记下开始读数为V1mL;E、在锥形瓶下垫一张白纸,滴定到终点,记录读数为V2mL.回答下列问题:
(1)正确的操作步骤的顺序是(用字母填写): → → →D→ .
(2)操作E中在锥形瓶下垫一张白纸的作用是 .
(3)若酸式滴定管没有用标准盐酸润洗,会对中和滴定结果有何影响? (填“偏高”、“偏低”或“无影响”).
该同学先配制0.55mol/L的NaOH溶液并测定其准确浓度.其操作步骤如下:A、在250mL的容量瓶中定容配成250mL烧碱溶液;B、用移液管移取25mL烧碱溶液于锥形瓶中并滴加几滴甲基橙指示剂;C、在天平上准确称取烧碱样品5.5g,在烧杯中加蒸馏水溶解;D、将标准盐酸溶液装入酸式滴定管,调整液面,并记下开始读数为V1mL;E、在锥形瓶下垫一张白纸,滴定到终点,记录读数为V2mL.回答下列问题:
(1)正确的操作步骤的顺序是(用字母填写):
(2)操作E中在锥形瓶下垫一张白纸的作用是
(3)若酸式滴定管没有用标准盐酸润洗,会对中和滴定结果有何影响?
考点:中和热的测定
专题:实验题
分析:(1)实验时应先称量一定质量的固体,溶解后配制成溶液,量取待测液与锥形瓶中,然后用标准液进行滴定;
(2)根据锥形瓶下垫一张白纸使滴定终点颜色变化更明显,便于分辨;
(3)未用标准液润洗滴定管,消耗盐酸体积偏大,测定结果偏高;
(2)根据锥形瓶下垫一张白纸使滴定终点颜色变化更明显,便于分辨;
(3)未用标准液润洗滴定管,消耗盐酸体积偏大,测定结果偏高;
解答:
解:(1)实验时应先称量一定质量的固体,溶解后配制成溶液,量取待测液与锥形瓶中,然后用标准液进行滴定,所以正确的操作步骤的顺序是C→A→B→D→E,
故答案为:C;A;B;E;
(2)因锥形瓶下垫一张白纸使滴定终点颜色变化更明显,便于分辨,
故答案为:使滴定终点颜色变化更明显,便于分辨;
(3)未用标准液润洗酸式滴定管,导致标准液的浓度减小,滴定消耗的标准液体积偏大,测定结果偏高,
故答案为:偏大;
故答案为:C;A;B;E;
(2)因锥形瓶下垫一张白纸使滴定终点颜色变化更明显,便于分辨,
故答案为:使滴定终点颜色变化更明显,便于分辨;
(3)未用标准液润洗酸式滴定管,导致标准液的浓度减小,滴定消耗的标准液体积偏大,测定结果偏高,
故答案为:偏大;
点评:本题主要考查了中和滴定操作以及误差分析,题目难度不大.注意在学习中把握相关基本实验方法,学习中注意积累.

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
各组混合物,不管它们以任何比例混合,只要总质量固定,完全燃烧后所得的CO2的量为常量,则该组有机物为( )
| A、甲醛和乙酸 |
| B、丁烯和丁烷 |
| C、甲醇和乙醇 |
| D、乙醇和乙醚 |
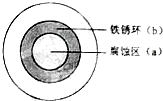 将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆圈中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示.导致现象的主要原因是液滴之下氧气含量比边缘处少.下列说法正确的是( )
将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆圈中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示.导致现象的主要原因是液滴之下氧气含量比边缘处少.下列说法正确的是( )| A、液滴中的Cl - 由a区向b区迁移 |
| B、铁腐蚀严重的区域,生锈也严重 |
| C、液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH- 形成Fe(OH)2,进一步氧化、脱水形成铁锈 |
| D、液滴边缘是正极区,发生的电极反应为:O2+2H2O+4e-=4OH- |
下列溶液中微粒的物质的量浓度关系一定正确的是( )
| A、pH=3的盐酸溶液和pH=11的氨水等体积混合:c(Cl-)>c(NH4+)>c(OH-)>c(H+) | ||||
B、0.1 mol?L-1 NaHCO3溶液中:c(Na+)+c(H+)=c(HCO
| ||||
| C、物质的量浓度相等的HF和NaF溶液等体积混合后有:c(Na+)=c(HF)+c(F-) | ||||
| D、0.1 mol?L-1 NaHS溶液中:c(Na+)=c(S2-)+c(HS-)+c(H2S) |

 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.