题目内容
19.关于a:0.1mol/L NH4Cl溶液和b:0.1mol/L NH3•H2O溶液,下列说法不正确的是( )| A. | 两溶液中存在的微粒种类:a>b | B. | c(NH4+):a>b | ||
| C. | c(OH-):a<b | D. | 水电离出的c(H+):a<b |
分析 0.1mol/L NH4Cl溶液显酸性,溶液中存在的离子有NH4+、NH3•H2O、H+、OH-、Cl-,0.1mol/L NH3•H2O溶液显碱性,溶液中存在的离子有NH4+、NH3•H2O、H+、OH-,能水解的盐促进水的电离,碱抑制水的电离,据此分析.
解答 解:A.0.1mol/L NH4Cl溶液显酸性,溶液中存在的离子有NH4+、NH3•H2O、H+、OH-、Cl-,0.1mol/L NH3•H2O溶液显碱性,溶液中存在的离子有NH4+、NH3•H2O、H+、OH-,所以两溶液中存在的微粒种类:a>b,故A正确;
B.一般水解程度较小,所以c(NH4+):a>b,故B正确;
C.0.1mol/L NH4Cl溶液显酸性,0.1mol/L NH3•H2O溶液显碱性,则c(OH-):a<b,故C正确;
D.NH4Cl促进水的电离,NH3•H2O会抑制水的电离,所以水的电离程度a>b,则水电离出的c(H+):a>b,故D错误.
故选D.
点评 本题考查盐类水解及弱电解质电离,明确弱电解质电离特点以及溶液中电荷守恒和物料守恒是解本题关键,题目难度中等,侧重于考查学生的分析能力.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
9.下列叙述正确的是( )
| A. | 用氨水清除试管壁附着的银镜 | |
| B. | 用氢氧化钠溶液清洗沾在皮肤上的苯酚 | |
| C. | 用食醋清除暖瓶水垢(主要成分碳酸钙) | |
| D. | 用碳酸钠溶液清除钢铁制品表面的铁锈 |
7.下列说法正确的是( )
| A. | 反应2H2(g)+O2(g)═2H2O(l) 在室温下可自发进行,则该反应的△H<0 | |
| B. | 常温常压下,7.8gNa2O2与水完全反应,产生1.12L气体 | |
| C. | 煤的干馏是物理变化,石油的裂化是化学变化 | |
| D. | 气体分子总数不再改变时,反应H2(g)+I2(g)?2HI(g))达到平衡 |
14.短周期主族元素W、X、Y、Z的原子序数依次增大.W、Z同族,Y、Z位于同周期且相邻,W、Y、Z三种元素原子的最外层电子数之和为11,X原子最外层电子数等于最内层电子数的一半.下列说法正确的是( )
| A. | W的最高价氧化物是大气污染物之一 | |
| B. | X、Y、Z的离子半径逐渐增大 | |
| C. | X的最高价氧化物的水化物能分别与Y、Z的最高价氧化物对应水化物反应 | |
| D. | 最简单氢化物的热稳定性:Z>W |
11.设NA为阿伏加德罗常数的值.下列有关叙述正确的是( )
| A. | 20 g D2O含有的中子数为8NA | |
| B. | 25℃时,l L pH=2的H2SO3溶液中所含H+数为0.01 NA | |
| C. | 标准状况下,22.4 L CH3OH中含有的共价键数为5 NA | |
| D. | 0.1 mol Cl2溶于水,转移电子数目为0.1 NA |
8.下列有关实验基本操作的说法正确的是( )
| A. | 用裂化汽油萃取溴水中的溴,将有机层从分液漏斗上口倒出 | |
| B. | 制备氢氧化亚铁时将装有NaOH溶液的胶头滴管插入液面深处并挤压 | |
| C. | 向蔗糖水解后的产物中加入银氨溶液,加热,检验蔗糖是否水解 | |
| D. | 将饱和FeCl3溶液滴入NaOH溶液中制备Fe(OH)3 |
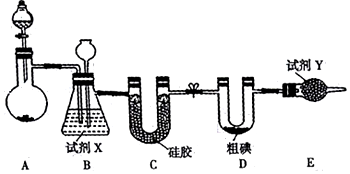
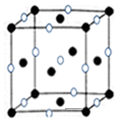 已知A、B、C、D、E、F是周期表前四周期的元素,原子序数依次增大.A的基态原子2p能级有2个单电子;C占整个地壳质量的48.6%,是地壳中含量最多的元素;E的单质常温常压下为黄绿色气体,化学性质十分活泼,具有毒性;F位于ds区,最外能层有单电子,是唯一的能大量天然产出的金属;D与F不同周期,但最外能层电子数相等.
已知A、B、C、D、E、F是周期表前四周期的元素,原子序数依次增大.A的基态原子2p能级有2个单电子;C占整个地壳质量的48.6%,是地壳中含量最多的元素;E的单质常温常压下为黄绿色气体,化学性质十分活泼,具有毒性;F位于ds区,最外能层有单电子,是唯一的能大量天然产出的金属;D与F不同周期,但最外能层电子数相等.