题目内容
5.近年来,国际原油价格大幅上涨,促使各国政府加大生物能源生产,其中乙醇汽油已进入实用化阶段.(1)乙醇官能团的电子式为
 ;
;(2)乙醇在铜或银做催化剂的条件下,可以被空气中的氧气氧化成X,该反应的化学方程式是2C2H5OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
(3)乙醇可以被直接氧化成Y(Mr=60),需要加入的试剂是酸性KMnO4溶液或酸性K2Cr2O7溶液;在浓硫酸作用下,乙醇与Y反应可生成一种有香味的物质W,该反应的类型为酯化(取代)反应;
(4)现有两瓶无色液体,分别盛有Y、W,只用一种试剂就可以鉴别,该试剂可以是ACE
A.水 B.乙醇 C.紫色石蕊试液 D.苯 E.碳酸钠溶液
(5)工业上通过乙烯与水在一定条件下反应制得乙醇,反应类型是加成反应,现代石油化工采用银做催化剂,乙烯能被氧气氧化生成M.该反应的原子利用率为100%,反应的化学方程式为2CH2=CH2+O2$→_{△}^{Ag}$
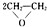 ;
;(6)乙醇-氧气燃料电池是以KOH溶液作为电解质溶液,写出其负极的电极反应式C2H5OH+16OH--12e-=2CO32-+11H2O.
分析 (1)乙醇的官能团为-OH;
(2)乙醇催化氧化生成乙醛;
(3)乙醇可以被直接氧化成Y(Mr=60),Y为CH3COOH,需要强氧化剂,且乙醇与乙酸可发生酯化反应;
(4)乙酸具有酸性,乙酸乙酯不溶于水;
(5)乙烯与水发生加成反应生成乙醇,乙烯能被氧气氧化生成M.该反应的原子利用率为100%,生成环氧乙烷;
(6)负极上乙醇失去电子.
解答 解:(1)乙醇含有羟基,羟基电子式为 ,故答案为:
,故答案为: ;
;
(2)乙醇在铜做催化剂的条件下可被氧气氧化为乙醛,反应的化学方程式为2C2H5OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
故答案为:2C2H5OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
(3)乙醇可以被直接氧化成Y(Mr=60),Y为CH3COOH,需要加入的试剂为酸性KMnO4溶液或酸性K2Cr2O7溶液,在浓硫酸作用下,乙醇与Y反应可生成一种有香味的物质W,该反应的类型为酯化(取代)反应,
故答案为:酸性KMnO4溶液或酸性K2Cr2O7溶液;酯化(取代)反应;
(4)A.乙酸溶于水,乙酸乙酯不溶于水,则利于水可鉴别,故A正确;
B.二者均与乙醇不反应,现象相同,不能鉴别,故B错误;
C.乙酸遇紫色石蕊试液变红,乙酸乙酯不能,现象不同可鉴别,故C正确;
D.均与苯不反应,不能鉴别,故D错误;
E.碳酸钠与乙酸反应生成气体,与乙酸乙酯不反应,现象不同可鉴别,故E正确;
故答案为:ACE;
(5)乙烯与水发生加成反应生成乙醇,乙烯能被氧气氧化生成环氧乙烷,根据质量守恒定律该反应为2CH2=CH2+O2$→_{△}^{Ag}$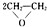 ,
,
故答案为:加成反应;2CH2=CH2+O2$→_{△}^{Ag}$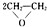 ;
;
(6)乙醇在负极发生氧化反应生成碳酸根离子和水,负极反应为C2H5OH+16OH--12e-=2CO32-+11H2O,故答案为:C2H5OH+16OH--12e-=2CO32-+11H2O.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意乙醇的性质及应用,综合性较强,题目难度不大.

 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案| A. | 门捷列夫 | B. | 阿伏伽德罗 | C. | 汤姆生 | D. | 道尔顿 |
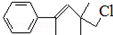 ,关于该有机物下列叙述正确的是( )
,关于该有机物下列叙述正确的是( )| A. | 分子式为C13H18Cl | |
| B. | 能使酸性KMnO4溶液褪色,但不能使溴水褪色 | |
| C. | 在加热和催化剂作用下,最多能和3mol H2反应 | |
| D. | 该分子中能通过聚合反应生成高分子化合物 |
| 实验操作 | 实验目的 | |
| A | 将卤代烃加入到热NaOH溶液中一段时间后,取上层液体,加入AgNO3液产生沉淀 | 证明卤代烃中含有卤元素 |
| B | 电石与水反应制得的气体直接通往酸性KMnO4溶液 | 证明制得的气体是否为乙炔 |
| C | 淀粉在硫酸催化作用下水解,将新制氢氧化铜悬浊液加入到水解后的溶液中 | 检验淀粉水解的产物葡萄糖 |
| D | 向纯碱中滴加醋酸,将产生的气体先通入饱和碳酸氢钠溶液再通入苯酚钠浓溶液 | 证明酸性:醋酸>碳酸>苯酚 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 常温下,100g46%乙醇水溶液中含有H原子数为12 NA | |
| B. | 23gNa与足量O2反应,生成Na2O 和Na2O2的混合物,转移的电子数为 NA | |
| C. | 标准状况下,2.24 LCCl4含有的共价键数为0.4 NA | |
| D. | 1 molN2与4molH2反应生成的NH3分子数小于2 NA |
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 放热反应在常温下一定很容易发生 | |
| C. | 吸热反应不加热不可能进行反应 | |
| D. | 反应是吸热还是放热是由反应物和生成物所具有的总能量的相对大小而决定的 |
| A. | 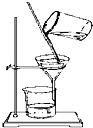 | B. | 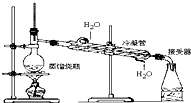 | ||
| C. |  | D. | 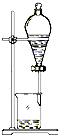 |
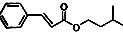 )是一种香料,一种合成路线如下:
)是一种香料,一种合成路线如下: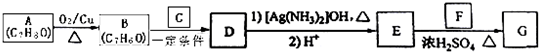
 ;
;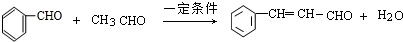 .
.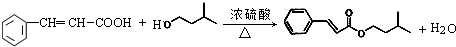 ,反应类型为酯化反应或取代反应.
,反应类型为酯化反应或取代反应.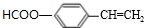 、
、 (写结构简式)
(写结构简式)