题目内容
下列有关溶液组成的描述合理的是
A.0.1mol·L-1FeCl3溶液中能大量存在Fe2+、NH4+、SCN一、SO42-
B.酸性溶液中可能大量存在Na+、ClO一、SO42-、I—
C.碱性溶液中能大量存在Mg2+、Cu2+、SO42-、NO3—
D.加入铝粉能产生氢气的溶液中可能大量存在NH4+、Fe2+、SO42-、Cl一
D
【解析】
试题分析:A、0.1mol·L-1FeCl3溶液中SCN一不能大量共存,二者反应使溶液显红色,A错误;B、酸性溶液中ClO一、I—发生氧化还原反应,不能大量共存,B错误;C、碱性溶液中Mg2+、Cu2+均不能大量共存,C错误;D、加入铝粉能产生氢气的溶液可能显酸性,也可能显碱性。如果显酸性,则可能大量存在NH4+、Fe2+、SO42-、Cl一,D正确,答案选D。
考点:考查离子共存的正误判断

二甲醚(CH3OCH3)是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上以CO和H2为原料生产二甲醚CH3OCH3的新工艺主要发生三个反应:
① CO(g) + 2H2(g) CH3OH(g) △H1=-Q1 kJ·mol-1
CH3OH(g) △H1=-Q1 kJ·mol-1
② 2CH3OH(g) CH3OCH3(g)+ H2O(g) △H2=-Q2 kJ·mol-1
CH3OCH3(g)+ H2O(g) △H2=-Q2 kJ·mol-1
③ CO(g)+ H2O(g) CO2(g) + H2(g) △H3=-Q3 kJ·mol-1
CO2(g) + H2(g) △H3=-Q3 kJ·mol-1
回答下列问题:
(1)新工艺的总反应3H2(g)+ 3CO(g) CH3OCH3(g)+ CO2(g)的热化学方程式为_________。
CH3OCH3(g)+ CO2(g)的热化学方程式为_________。
(2)工业上一般在恒容密闭容器中采用下列反应合成甲醇:CO(g) + 2H2(g) CH3OH (g) △H
CH3OH (g) △H
下表所列数据是该反应在不同温度下的化学平衡常数(Κ)。
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
① 由表中数据判断ΔH 0 (填“ >”、“=”或“<”)。能够说明某温度下该反应是平衡状态的是
A.体系的压强不变
B.密度不变
C.混合气体的相对分子质量不变
D.c(CO)=c(CH3OH)
② 某温度下,将 2mol CO和 6mol H2 充入2L的密闭容器中,充分反应 10min后,达到平衡时测得c(CO)=0.2mol/L,计算此温度下的平衡常数K= 。
(3)工业生产是把水煤气中的混合气体经过处理后获得的较纯H2用于合成氨。合成氨反应原理为:N2(g)+3H2(g)  2NH3(g) ΔH=-92.4kJ?mol-1。实验室模拟化工生产,在恒容密闭容器中冲入一定量N2和H2后,分别在不同实验条件下反应,N2浓度随时间变化如下图。
2NH3(g) ΔH=-92.4kJ?mol-1。实验室模拟化工生产,在恒容密闭容器中冲入一定量N2和H2后,分别在不同实验条件下反应,N2浓度随时间变化如下图。

请回答下列问题:
①与实验Ⅰ比较,实验Ⅱ改变的条件为 。
②在实验Ⅲ中改变条件为采用比实验Ⅰ更高的温度,请在下图中画出实验I和实验Ⅲ中NH3浓度随时间变化的示意图。

下列各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是
组别 | 甲 | 乙 | 丙 |
A | Mg | FeSO4 | O2 |
B | Al2O3 | HCl | NaOH |
C | CO2 | H2O | Na2O2 |
D | NaHCO3 | Ca(OH)2 | Na2CO3 |
 H2(g)+
H2(g)+ 296kJ·mol
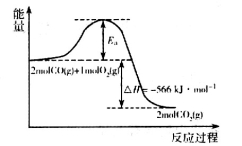
296kJ·mol 。
。
 (未配平)。
(未配平)。
 物质
物质