题目内容
常温条件下,下列溶液中的各组离子一定能够大量共存的是( )
| A、pH=1的溶液:Na+、Fe2+、Cl-、NO3- | ||
| B、含有大量I-的溶液:ClO-、Na+、Cl-、CO32- | ||
C、
| ||
| D、加入铝粉能放出大量H2的溶液:K+、NH4+、SO42-、CO32- |
考点:离子共存问题
专题:离子反应专题
分析:A.pH=1的溶液呈酸性;
B.I-具有还原性,与氧化性离子不能大量共存;
C.
=1010mol?L-1的溶液呈酸性;
D.加入铝粉能放出大量H2的溶液,可能为强碱性或非氧化性酸溶液.
B.I-具有还原性,与氧化性离子不能大量共存;
C.
| c(H+) |
| c(OH-) |
D.加入铝粉能放出大量H2的溶液,可能为强碱性或非氧化性酸溶液.
解答:
解:A.pH=1的溶液呈酸性,酸性条件下Fe2+、NO3-发生氧化还原反应,故A错误;
B.I-具有还原性,与ClO-发生氧化还原反应,不能大量共存,故B错误;
C.
=1010mol?L-1的溶液呈酸性,离子之间不发生任何反应,可大量共存,故C正确;
D.加入铝粉能放出大量H2的溶液,可能为强碱性或非氧化性酸溶液,碱性条件下NH4+不能大量共存,酸性条件下CO32-不能大量共存,故D错误.
故选C.
B.I-具有还原性,与ClO-发生氧化还原反应,不能大量共存,故B错误;
C.
| c(H+) |
| c(OH-) |
D.加入铝粉能放出大量H2的溶液,可能为强碱性或非氧化性酸溶液,碱性条件下NH4+不能大量共存,酸性条件下CO32-不能大量共存,故D错误.
故选C.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子的颜色、离子之间的反应为解答的关键,侧重复分解反应及氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
下列事实中,不能用勒夏特列原理解释的是( )
| A、盛有NO2和N2O4 混合气体的烧瓶置于热水中,气体颜色变深 |
| B、工业合成氨选择500℃左右的温度比室温有利 |
| C、实验室中常用排饱和食盐水的方法收集Cl2 |
| D、合成氨时采用循环操作及将氨液化分离,可提高原料的利用率 |
下列物质,不能作为从溴水中萃取溴的溶剂的是( )
| A、四氯化碳 | B、酒精 |
| C、苯 | D、二氯甲烷 |
符合下列分子式的有机物没有同分异构现象的是( )
| A、CH4 |
| B、C12H22O11 |
| C、C4H10 |
| D、C4H9OH |
在4L密闭容器中充入6mol A气体和5mol B气体,在一定条件下发生反应:3A(g)+B(g)?2C(g)+xD(g),达到平衡时,生成了2mol C,经测定D的浓度为0.5mol?L-1,下列判断正确的是( )
| A、X=3 |
| B、A的转化率为50% |
| C、平衡时B的浓度为1.5 mol?L-1 |
| D、达到平衡时,在相同温度下容器内混合气体的压强是反应前的95% |
可逆反应mA(g)?nB(g)+pC(s)△H=QKJ/moL,温度和压强的变化对正、逆反应速率的影响分别符合图中的两个图象,以下叙述正确的是( )


| A、m>n,Q>0 |
| B、m<n+p,Q>0 |
| C、m>n,Q<0 |
| D、m>n+p,Q<0 |
 ”表示上述相关元素的原子中除去最外层电子的剩余部分,“
”表示上述相关元素的原子中除去最外层电子的剩余部分,“ ”表示没有形成共价键的最外层电子,短线表示共价键.
”表示没有形成共价键的最外层电子,短线表示共价键.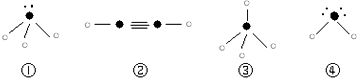
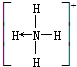 (→表示共用电子对由N原子单方面提供). 请画出N4H44+的结构式
(→表示共用电子对由N原子单方面提供). 请画出N4H44+的结构式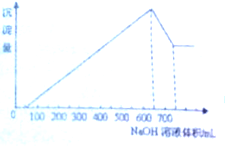 将一定量的氧化铝和氧化铁的混合物完全溶解100mL某浓度的硫酸中,而后向其中逐滴加入1mol/L的NaOH溶液,产生沉淀的量与加入NaOH的体积关系如图(图中横坐标每个格子表示50mL)则:
将一定量的氧化铝和氧化铁的混合物完全溶解100mL某浓度的硫酸中,而后向其中逐滴加入1mol/L的NaOH溶液,产生沉淀的量与加入NaOH的体积关系如图(图中横坐标每个格子表示50mL)则: