题目内容
16.下列说法正确的是( )| A. | 反应热就是反应中放出的能 | |
| B. | 在101 kPa时,1 mol碳燃烧所放出的热量为碳的燃烧热 | |
| C. | 由C(s,石墨)=C(s,金刚石),△H=1.9 kJ•mol-1可知,金刚石比石墨稳定 | |
| D. | 等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多 |
分析 A.反应热是在化学反应过程中放出或吸收的热量;
B.在101kPa时,1mol碳完全燃烧生成二氧化碳气体时所放出的热量碳的燃烧热;
C.石墨转化为金刚石属于吸热反应,说明等物质的量的石墨的能量低于金刚石的能量;
D.固体硫转化为蒸汽硫需要吸热.
解答 解:A.在化学反应过程中放出或吸收的热量,通常叫反应热,故A错误;
B.在101kPa时,1mol碳完全燃烧生成二氧化碳气体时所放出的热量碳的燃烧热,若不完全燃烧放出的热量就不是碳的燃烧热,故B错误;
C.石墨转化为金刚石属于吸热反应,说明等物质的量的石墨的能量低于金刚石的能量,因此石墨比金刚石稳定,故C错误;
D.蒸汽硫转化为固体硫需要放热,等量的硫蒸气和硫固体分别完全燃烧,产物相同,因此前者放出的热量多,故D正确;
故选D.
点评 本题考查了反应热的定义、分类和意义,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意燃烧热的定义中要求生成稳定的氧化物.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
1.下列说法正确的是( )
| A. | 新制的氯水保存在无色玻璃瓶中 | |
| B. | 氢气在氯气中燃烧生成白色烟雾 | |
| C. | 常温下,浓硝酸可用铝罐来贮存,说明浓硝酸具有强氧化性 | |
| D. | 向蔗糖中加入浓硫酸后出现发黑现象,说明浓H2SO4具有吸水性 |
11.短周期元素X、Y、Z、W在周期表中的相对位置如右图所示,已知它们的最外层电子数之和为21,下列说法错误的是( )


| A. | 原子半径由大到小的顺序:X、Y、Z、W | |
| B. | 元素最高正价由低到高的顺序:X、Y、Z、W | |
| C. | 简单氢化物的热稳定性由弱到强的顺序:Y、Z、W | |
| D. | 最高价氧化物的水化物的酸性由弱到强的顺序:X、Y、Z |
1.如图是元素周期表的一部分
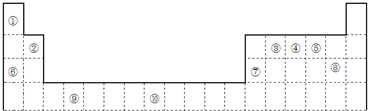
(1)元素⑩的次外层电子数为14个.
(2)如果在温度接近373K时,根据M=m/n测定⑤的气态氢化物的相对分子质量,结果发现测定结果比理论值高,其原因是分子间存在氢键,H2O分子发生缔合;
(3)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的氢氧化物有相似的性质.写出元素②的氢氧化物与NaOH溶液反应的离子方程式2OH-+Be(OH)2=BeO22-+2H2O;
(4)根据下列五种元素的第一至第四电离能数据(单位:kJ•mol-1),回答下面各题:
①在周期表中,最可能处于同一主族的是R和U.(填元素代号)
②T元素最可能是p(填“s”、“p”、“d”、“ds”等)区元素;若T为第二周期元素,Z是第三周期元素中原子半径最小的主族元素,则T、Z形成的化合物分子键角为120°.

(1)元素⑩的次外层电子数为14个.
(2)如果在温度接近373K时,根据M=m/n测定⑤的气态氢化物的相对分子质量,结果发现测定结果比理论值高,其原因是分子间存在氢键,H2O分子发生缔合;
(3)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的氢氧化物有相似的性质.写出元素②的氢氧化物与NaOH溶液反应的离子方程式2OH-+Be(OH)2=BeO22-+2H2O;
(4)根据下列五种元素的第一至第四电离能数据(单位:kJ•mol-1),回答下面各题:
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
②T元素最可能是p(填“s”、“p”、“d”、“ds”等)区元素;若T为第二周期元素,Z是第三周期元素中原子半径最小的主族元素,则T、Z形成的化合物分子键角为120°.
6.下列说法中正确的是( )
| A. | PM 2.5、二氧化碳都属于空气质量日报的内容 | |
| B. | 向煤中加入适量CaSO4,可大大减少燃烧产物中SO2的量 | |
| C. | 对“地沟油”进行分馏可得到汽油;玻璃、水泥和陶瓷都属于传统硅酸盐材料 | |
| D. | “光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化台物有关 |
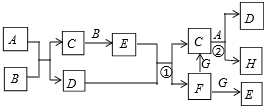 下列有关物质的转化关系如图所示(部分物质与条件已略去,其中反应②的条件是“700℃,催化剂”).G是常见的红色金属单质,B、H是空气的主要成分,A、C、E均是常见气体,D是最常见的无色液体.请回答下列问题:
下列有关物质的转化关系如图所示(部分物质与条件已略去,其中反应②的条件是“700℃,催化剂”).G是常见的红色金属单质,B、H是空气的主要成分,A、C、E均是常见气体,D是最常见的无色液体.请回答下列问题: .
. 元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.
元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.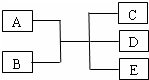 已知A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,它们之间有如下反应关系.
已知A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,它们之间有如下反应关系.