题目内容
6.下列说法中正确的是( )| A. | PM 2.5、二氧化碳都属于空气质量日报的内容 | |
| B. | 向煤中加入适量CaSO4,可大大减少燃烧产物中SO2的量 | |
| C. | 对“地沟油”进行分馏可得到汽油;玻璃、水泥和陶瓷都属于传统硅酸盐材料 | |
| D. | “光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化台物有关 |
分析 A.空气质量日报的内容包括有害气体和颗粒物;
B.要减少燃烧产物中SO2的量,通常向煤中加入适量石灰石或生石灰;煤中加入CaSO4不能减少燃烧产物中SO2的量,因为CaSO4与SO2不反应;
C.“地沟油”的成分主要成分是油脂,即高级脂肪酸甘油酯,汽油的成分是烃;
D.以一氧化氮和二氧化氮为主的氮氧化物是形成光化学烟雾和硝酸型酸雨的一个重要原因.
解答 解:A.二氧化碳是无毒气体,不属于空气质量日报的内容,故A错误;
B.因为CaSO4与SO2不反应,所以在煤中加入CaSO4,不能减少燃烧产物中SO2的量;要减少燃烧产物中SO2的量,通常向煤中加入适量石灰石或生石灰,故B错误;
C.“地沟油”的成分主要是油脂,即高级脂肪酸甘油酯,汽油的成分是烃,故地沟油分馏不能得到汽油,故C错误;
D.以一氧化氮和二氧化氮为主的氮氧化物是形成“光化学烟雾”“硝酸型酸雨”的形成的一个重要原因,故D正确.
故选D.
点评 本题考查化学与环境、材料、信息、能源关系密切相关的知识,涉及生产、生活有关的地沟油、大气污染等,为高频考点,侧重于基础知识的综合理解和运用的考查,难度不大.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案
相关题目
16.下列说法正确的是( )
| A. | 反应热就是反应中放出的能 | |
| B. | 在101 kPa时,1 mol碳燃烧所放出的热量为碳的燃烧热 | |
| C. | 由C(s,石墨)=C(s,金刚石),△H=1.9 kJ•mol-1可知,金刚石比石墨稳定 | |
| D. | 等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多 |
17.下列性质中,不能说明乙酸是弱电解质的是( )
①乙酸溶液能导电
②常温时,0.1mol/L乙酸溶液的pH约为3
③乙酸能和碳酸钙反应放出CO2
④10mL 1mol/L乙酸溶液与10mL 1mol/L的NaOH溶液恰好完全反应
⑤同pHH的盐酸和乙酸分别与足量铁片反应,乙酸产生H2多
⑥pH=1的醋酸溶液用水稀释1000倍后,pH<4.
①乙酸溶液能导电
②常温时,0.1mol/L乙酸溶液的pH约为3
③乙酸能和碳酸钙反应放出CO2
④10mL 1mol/L乙酸溶液与10mL 1mol/L的NaOH溶液恰好完全反应
⑤同pHH的盐酸和乙酸分别与足量铁片反应,乙酸产生H2多
⑥pH=1的醋酸溶液用水稀释1000倍后,pH<4.
| A. | ①②③ | B. | ④⑤⑥ | C. | ①③④ | D. | ②③④ |
1.下列做法正确的是( )
| A. | 将浓硝酸保存在无色玻璃瓶中 | |
| B. | 金属钠和钾保存在煤油中 | |
| C. | Na2CO3可以保存在玻璃塞的玻璃瓶中 | |
| D. | NaOH固体放在滤纸上称量 |
11.对H2O的电离平衡不产生影响的粒子是( )
| A. |  | B. | Fe3+ | C. | 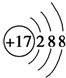 | D. | 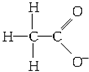 |
18.下表是不同温度下水的离子积常数:
试回答以下问题:
(1)T2℃时,将pH=11的苛性钠溶液V1 L与pH=1的稀硫酸V2 L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1:V2=9:11,此溶液中各种离子的浓度由大到小的顺序是c(Na+)>c(SO42-)>c(H+)>c(OH-).
(2)25℃时,用0.01mol/LNaOH溶液滴定0.02mol/L 的硫酸,中和后加蒸馏水稀释到5mL,若滴定时终点判断有误差;①多加了1滴NaOH溶液②少加1滴NaOH溶(设1滴为0.05mL),则①和②溶液中c(OH-)之比是106:1.
(3)25℃时,0.1mol/L的NaHCO3溶液的pH为8,同浓度的NaAlO2溶液的pH为11.将两种溶液等体积混合,可能发生的现象白色沉淀_此空删去其主要原因是(用离子方程式表示)HCO3-+AlO2-+H2O=Al(OH)3↓+CO32-_.
(4)含有Cr2O${\;}_{7}^{2-}$的废水毒性较大,某工厂废水中含5.00×10-3 mol•L-1的Cr2O${\;}_{7}^{2-}$.为使废水能达标排放,做如下处理:Cr2O${\;}_{7}^{2-}$$→_{H+}^{绿矾}$Cr3+、Fe3+$\stackrel{石灰水}{→}$Cr(OH)3、Fe(OH)3.欲使10L该废水中的Cr2O${\;}_{7}^{2-}$完全转化为
Cr3+,则理论上需要加入83.4 g FeSO4•7H2O.若处理后的废水中残留的c(Fe3+)=2×10-13 mol•L-1,则残留的Cr3+的浓度为3×10-6 mol•L-1(已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31).
| 温度/℃ | 25 | T2 |
| 水的离子积常数 | 1×10-14 | 1×10-12 |
(1)T2℃时,将pH=11的苛性钠溶液V1 L与pH=1的稀硫酸V2 L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1:V2=9:11,此溶液中各种离子的浓度由大到小的顺序是c(Na+)>c(SO42-)>c(H+)>c(OH-).
(2)25℃时,用0.01mol/LNaOH溶液滴定0.02mol/L 的硫酸,中和后加蒸馏水稀释到5mL,若滴定时终点判断有误差;①多加了1滴NaOH溶液②少加1滴NaOH溶(设1滴为0.05mL),则①和②溶液中c(OH-)之比是106:1.
(3)25℃时,0.1mol/L的NaHCO3溶液的pH为8,同浓度的NaAlO2溶液的pH为11.将两种溶液等体积混合,可能发生的现象白色沉淀_此空删去其主要原因是(用离子方程式表示)HCO3-+AlO2-+H2O=Al(OH)3↓+CO32-_.
(4)含有Cr2O${\;}_{7}^{2-}$的废水毒性较大,某工厂废水中含5.00×10-3 mol•L-1的Cr2O${\;}_{7}^{2-}$.为使废水能达标排放,做如下处理:Cr2O${\;}_{7}^{2-}$$→_{H+}^{绿矾}$Cr3+、Fe3+$\stackrel{石灰水}{→}$Cr(OH)3、Fe(OH)3.欲使10L该废水中的Cr2O${\;}_{7}^{2-}$完全转化为
Cr3+,则理论上需要加入83.4 g FeSO4•7H2O.若处理后的废水中残留的c(Fe3+)=2×10-13 mol•L-1,则残留的Cr3+的浓度为3×10-6 mol•L-1(已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31).
15.实验室制取少量干燥的氨气涉及下列装置中,其中正确的是( )
| A. | 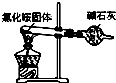 如图是氨气发生装置 | B. | 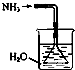 如图是氨气吸收装置 | ||
| C. | 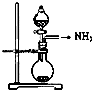 如图是氨气发生装置 | D. | 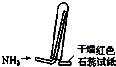 如图是氨气收集、检验装置 |
16.某主族元素在周期表中的位置,取决于元素原子的( )
| A. | 相对原子质量 | B. | 电子层数和核内中子数 | ||
| C. | 电子层数和最外层电子数 | D. | 金属性和非金属性的强弱 |