题目内容
16.在实验室中,用10gCaCO3与足量的稀盐酸反应.(1)至少需要2mol/L稀盐酸多少毫升?
(2)生成标准状况下的CO2多少升?
(3)生成CaCl2的物质的量是多少?
分析 发生反应:CaCO3+2HCl═CaCl2+CO2↑+H2O,根据n=$\frac{m}{M}$计算碳酸钙物质的量,根据方程式计算氯化钙、HCl、二氧化碳物质的量,由此分析解答.
解答 解:10g CaCO3 的物质的量=$\frac{10g}{100g/mol}$=0.1mol
CaCO3+2HCl═CaCl2+H2O+CO2↑
1 2 1 22.4L
0.1mol n(HCl) n(CaCl2) V(CO2)
n(HCl)=$\frac{0.1mol×2}{1}$=0.2mol,所以需要2mol/L稀盐酸的体积为:$\frac{0.2mol}{2mol/L}$=0.1L=100ml;
n(CaCl2)=$\frac{0.1mol×1}{1}$=0.1mol
V(CO2)=$\frac{0.1mol×22.4L}{1mol}$=2.24L
答:(1)至少需要2mol/L稀盐酸100ml;
(2)生成标准状况下的CO22.24L;
(3)生成CaCl2的物质的量是0.1mol.
点评 本题考查化学方程式的有关计算,比较基础,注意对基础知识的理解掌握.

练习册系列答案
相关题目
6.物质的结构决定物质的性质.请回答下列涉及物质结构和性质的问题:
(1)基态Cu2+的电子排布式为1s22s22p63s23p63d9,其M电子层的电子数为17.
(2)VSEPR理论认为价层电子对间互斥力(F)大小顺序:F(孤电子对间)>F(孤电子对-成键电子对)>F(成键电子对间),已知XeF4中Xe价层电子对数为6,其VSEPR模型为八面体,为使得价层电子对间的孤电子对斥力最小,预测XeF4分子中的键角应为90°.
(3)除NH3、H2O、HF外,同主族氢化物的沸点随周期数增大而升高的原因是同为分子晶体,物质的组成与结构相似,相对分子质量越大,分子间作用力越大,沸点越高;
已知NH3、H2O、HF的氢键键能和结构如表:
则如图1H2O、HF、NH3沸点由高到低的顺序依次为:H2O>HF>NH3.
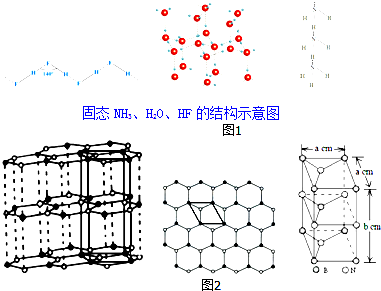
(4)石墨型BN呈白色,亦称“白石墨”.“白石墨”的结构示意图和晶胞如图2(中图是晶胞底面从“白石墨”中的截取情况),则“白石墨”中B和N的杂化方式分别为sp2和sp2,白石墨的密度为$\frac{100}{\sqrt{3}{N}_{A}{a}^{2}b}$g•cm-3( 已知相对原子质量B:11 N:14 阿伏加德罗常数的数值用NA表示).
(1)基态Cu2+的电子排布式为1s22s22p63s23p63d9,其M电子层的电子数为17.
(2)VSEPR理论认为价层电子对间互斥力(F)大小顺序:F(孤电子对间)>F(孤电子对-成键电子对)>F(成键电子对间),已知XeF4中Xe价层电子对数为6,其VSEPR模型为八面体,为使得价层电子对间的孤电子对斥力最小,预测XeF4分子中的键角应为90°.
(3)除NH3、H2O、HF外,同主族氢化物的沸点随周期数增大而升高的原因是同为分子晶体,物质的组成与结构相似,相对分子质量越大,分子间作用力越大,沸点越高;
已知NH3、H2O、HF的氢键键能和结构如表:
| 物质 | 氢键X-H…Y | 键能/kJ•mol-1 |
| (HF)n | F-H…F | 28.1 |
| 冰 | O-H…O | 18.8 |
| (NH3)n | N-H…N | 5.4 |

(4)石墨型BN呈白色,亦称“白石墨”.“白石墨”的结构示意图和晶胞如图2(中图是晶胞底面从“白石墨”中的截取情况),则“白石墨”中B和N的杂化方式分别为sp2和sp2,白石墨的密度为$\frac{100}{\sqrt{3}{N}_{A}{a}^{2}b}$g•cm-3( 已知相对原子质量B:11 N:14 阿伏加德罗常数的数值用NA表示).
7.胶体是一种微粒直径在1-100nm之间的分散系.下列事实与胶体的性质无关的是( )
| A. | 清晨在密林中看到一缕缕光束 | |
| B. | 盐酸与硝酸银溶液反应生成白色沉淀 | |
| C. | 豆浆中加入盐卤做豆腐 | |
| D. | 一束平行光射入蛋白质溶液中,侧面可看到一束光亮的通路 |
1.以下物质是按一定规律排列的,Mn、S、MnO2、SO2、K2MnO4、 ,则方框内的物质为( )
,则方框内的物质为( )
 ,则方框内的物质为( )
,则方框内的物质为( )| A. | H2S | B. | Na2SO3 | C. | CuSO4 | D. | Cu2S |
6.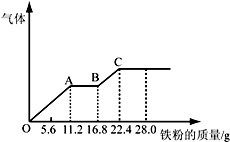 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )| A. | 混合酸中NO3-物质的量为0.2mol | |
| B. | OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气 | |
| C. | 第二份溶液中最终溶质为FeSO4 | |
| D. | H2SO4浓度为4mol•L-1 |
3.检验溴乙烷中含有溴元素存在的实验步骤、操作和顺序正确的是( )
①加入AgNO3溶液 ②加入NaOH溶液加热 ③加入适量HNO3 ④冷却.
①加入AgNO3溶液 ②加入NaOH溶液加热 ③加入适量HNO3 ④冷却.
| A. | ①②④③ | B. | ②④③① | C. | ②④① | D. | ②③④① |
4.将锌片和铜片用导线连接置于稀硫酸溶液中,下列各叙述正确的是( )


| A. | 锌片做负极,锌发生还原反应 | B. | 铜片做正极,铜得电子 | ||
| C. | 溶液中的pH值减小 | D. | 铜片上有气泡冒出 |
