题目内容
下列各组离子中,能在溶液中大量共存的是( )
| A、Na+、Cu2+、Cl-、SO42- |
| B、H+、Cl-、CO32-、SO42- |
| C、Ba2+、Na+、SO42-、Cl- |
| D、H+、K+、OH-、Cl- |
考点:离子共存问题
专题:
分析:A.Na+、Cu2+、Cl-、SO42-离子之间不满足离子反应发生条件;
B.氢离子与碳酸根离子反应生成二氧化碳气体和水;
C.钡离子与硫酸根离子反应生成难溶物硫酸钡;
D.氢离子与氢氧根离子反应生成弱电解质水.
B.氢离子与碳酸根离子反应生成二氧化碳气体和水;
C.钡离子与硫酸根离子反应生成难溶物硫酸钡;
D.氢离子与氢氧根离子反应生成弱电解质水.
解答:
解:A.Na+、Cu2+、Cl-、SO42-之间不发生反应,在溶液中能够大量共存,故A正确;
B.H+、CO32-之间反应生成二氧化碳和水,在溶液中不能大量共存,故B错误;
C.Ba2+、SO42-之间反应生成硫酸钡沉淀,在溶液中不能大量共存,故C错误;
D.H+、OH-离子之间反应生成水,在溶液中不能大量共存,故D错误;
故选A.
B.H+、CO32-之间反应生成二氧化碳和水,在溶液中不能大量共存,故B错误;
C.Ba2+、SO42-之间反应生成硫酸钡沉淀,在溶液中不能大量共存,故C错误;
D.H+、OH-离子之间反应生成水,在溶液中不能大量共存,故D错误;
故选A.
点评:本题考查离子共存的正误判断,该题是高考中的高频题,属于中等难度的试题,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
实验室从含溴化氢的废液中提取溴单质,下列说法中能达到实验目的是( )
A、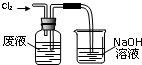 氧化废液中的溴化氢 |
B、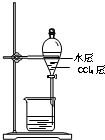 分离CCl4层和水层 |
C、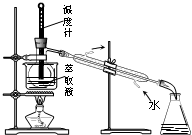 分离CCl4和液溴 |
D、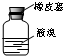 用仪器丁长期贮存液溴 |
下列叙述正确的是( )
| A、SiO2和A12O3都既能与酸反应,又能与碱反应 |
| B、硫化钠溶于水中发生反应的离子方程式为S2-+2H2O?H2S+2OH- |
| C、3.2 g Cu与5.5 mL l8.4 mol?L -1的浓H2SO4充分反应,转移的电子数为6.02×1022 |
| D、由水电离的c(H+)=1×10 -13mol?L -1的溶液中Cl-、HCO3-、NO3-、NH4+能大量共存 |
下列有关化学用语使用正确的是( )
A、硫原子的原子结构示意图: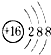 | ||
B、NH4Cl的电子式: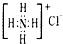 | ||
C、核内有8个中子的碳原子:
| ||
| D、HCO3-电离的离子方程式:HCO3-+H2O?CO32-+H3O+ |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O
3Zn(OH)2+2Fe(OH)3+4KOH.下列叙述不正确的是( )
| 放电 |
| 充电 |
| A、放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2 |
| B、充电时阳极反应为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O |
| C、放电时每转移3mol电子,正极有1molK2FeO4被氧化 |
| D、放电时的正极在充电时须接电源正极 |
