题目内容
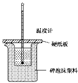 某实验小组学生按照课本实验要求,用50mL0.5mol?L-1盐酸与50mL0.55mol?L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量计算中和热.下列说法正确的是( )
某实验小组学生按照课本实验要求,用50mL0.5mol?L-1盐酸与50mL0.55mol?L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量计算中和热.下列说法正确的是( )| A、实验过程中没有热量损失 |
| B、图中实验装置缺少环形玻璃搅拌棒 |
| C、烧杯间填满碎泡沫塑料的作用是固定小烧杯 |
| D、酸或碱的物质的量越大,所测中和热的数值越大 |
考点:中和热的测定
专题:化学反应中的能量变化
分析:A.根据实验过程的保温情况确定保温效果;
B.根据量热计的构造来判断该装置的缺少仪器;
C.中和热测定实验成败的关键是保温工作,烧杯间填满碎纸条的作用是保温;
D.中和热是强酸和强碱反应生成1mol水时放出的热量,与酸碱的用量无关;
B.根据量热计的构造来判断该装置的缺少仪器;
C.中和热测定实验成败的关键是保温工作,烧杯间填满碎纸条的作用是保温;
D.中和热是强酸和强碱反应生成1mol水时放出的热量,与酸碱的用量无关;
解答:
解:A.该装置的保温效果并不如量热计那样好,肯定存在热量的散失,故A错误;
B.根据量热计的构造可知该装置的缺少仪器是环形玻璃搅拌器,故B正确;
C.中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是减少实验过程中的热量损失,故C错误;
D.因为中和热是指酸跟碱发生中和反应生成1molH2O所放出的热量,与酸碱的用量无关,中和热数值相等,故D错误;
故选B.
B.根据量热计的构造可知该装置的缺少仪器是环形玻璃搅拌器,故B正确;
C.中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是减少实验过程中的热量损失,故C错误;
D.因为中和热是指酸跟碱发生中和反应生成1molH2O所放出的热量,与酸碱的用量无关,中和热数值相等,故D错误;
故选B.
点评:本题考查中和热的测定,题目难度不大,注意理解中和热的概念是解题的关键.

练习册系列答案
相关题目
下列物质含分子最多的是( )
| A、1.204×1024个O2 |
| B、3molCO2 |
| C、标准状况下89.6LCl2 |
| D、标准状况下90mL水(水的密度为1g/mL) |
下列关于强、弱电解质的叙述,有错误的是( )
| A、电解质本身不一定能导电 |
| B、在溶液中,导电能力弱的电解质不一定是弱电解质 |
| C、纯净的强电解质在液态时,有的导电,有的不导电 |
| D、SO2的水溶液能导电,所以SO2是电解质 |
下列图示与对应的叙述相符的是( )
A、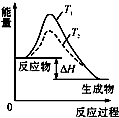 温度T1>T2,SO2与O2反应过程中的能量变化 |
B、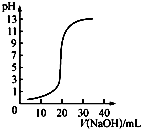 表示0.100 0 mol/L NaOH溶液滴定20.00 mL 0.100 0 mol/L CH3COOH溶液 |
C、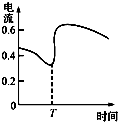 表示Zn、Cu和稀硫酸构成的原电池中电流强度的变化,T时加入了H2O2 |
D、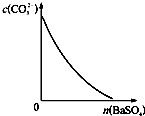 表示在饱和Na2CO3溶液中逐步加BaSO4固体后,溶液中c(CO32-)的浓度变化 |
下列有关实验的叙述,正确的是( )
| A、用广泛pH试纸测得氯水的pH为2 |
| B、用托盘天平称取10.50g干燥的NaCl固体 |
| C、配制一定物质的量浓度的溶液,定容时俯视容量瓶的刻度线,会使所配溶液的浓度偏高 |
| D、制备Fe(OH)2时,向FeSO4溶液中滴入NaOH溶液时,胶头滴管不能伸入液面以下 |
为验证甲烷分子中含有碳、氢两种元素,可将其燃烧产物通过①浓H2SO4;②澄清石灰水;③无水硫酸铜.正确的顺序是( )
| A、①②③ | B、②③ |
| C、②③① | D、③② |
 1L某混合溶液中,溶质X、Y的浓度都为0.1mol/L,向混合溶液中滴加某溶液Z(0.1mol/L的氢氧化钠或硫酸溶液),所得沉淀的物质的量随着Z溶液的体积变化关系如图所示,则X、Y、Z分别是( )
1L某混合溶液中,溶质X、Y的浓度都为0.1mol/L,向混合溶液中滴加某溶液Z(0.1mol/L的氢氧化钠或硫酸溶液),所得沉淀的物质的量随着Z溶液的体积变化关系如图所示,则X、Y、Z分别是( )| A、AlCl3、FeCl3、NaOH |
| B、AlCl3、MgCl2、NaOH |
| C、NaAlO2、Ba(OH)2、H2SO4 |
| D、NaAlO2、BaCl2、H2SO4 |