题目内容
下列图示与对应的叙述相符的是( )
A、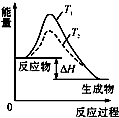 温度T1>T2,SO2与O2反应过程中的能量变化 |
B、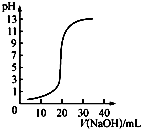 表示0.100 0 mol/L NaOH溶液滴定20.00 mL 0.100 0 mol/L CH3COOH溶液 |
C、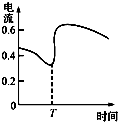 表示Zn、Cu和稀硫酸构成的原电池中电流强度的变化,T时加入了H2O2 |
D、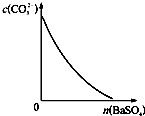 表示在饱和Na2CO3溶液中逐步加BaSO4固体后,溶液中c(CO32-)的浓度变化 |
考点:化学反应的能量变化规律,难溶电解质的溶解平衡及沉淀转化的本质,酸碱混合时的定性判断及有关ph的计算
专题:
分析:A.温度不能改变活化能的大小;
B.醋酸是弱酸,部分电离;
C.双氧水具有强氧化性;
D.沉淀不能完全转化.
B.醋酸是弱酸,部分电离;
C.双氧水具有强氧化性;
D.沉淀不能完全转化.
解答:
解:A.温度不能改变活化能的大小,活化能相同,故A错误;
B.0.1000mol?L-1 CH3COOH溶液的pH大于1,故B错误;
C.双氧水具有强氧化性,能加快反应速率,故C正确;
D.溶液中c(CO32-)的浓度不可能变为0,故D错误.
故选C.
B.0.1000mol?L-1 CH3COOH溶液的pH大于1,故B错误;
C.双氧水具有强氧化性,能加快反应速率,故C正确;
D.溶液中c(CO32-)的浓度不可能变为0,故D错误.
故选C.
点评:本题考查反应的能量变化、溶液的酸碱性、化学反应速率和沉淀转化,易错选B,这是由于图象的变化趋势是完全正确的,但却忽略了醋酸起始时的pH,因此认真审题,是答好试题的关键,难度不大.

练习册系列答案
相关题目
人们把食品分为绿色食品、蓝色食品、白色食品等.绿色植物通过光合作用转化的食品叫绿色食品,海洋提供的叫蓝色食品,通过微生物发酵制得的食品叫白色食品.下面属于白色食品的是( )
| A、酱油 | B、面粉 | C、海带 | D、菜油 |
下列离子方程式书写正确的是( )
| A、用醋酸除去水垢:CaCO3+2H+=Ca2++H2O+CO2↑ | ||||
B、用铜为电极电解饱和食盐水:2Cl-+2H2O
| ||||
| C、FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | ||||
| D、Ba(OH)2溶液中滴加过量NaHSO4:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
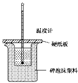 某实验小组学生按照课本实验要求,用50mL0.5mol?L-1盐酸与50mL0.55mol?L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量计算中和热.下列说法正确的是( )
某实验小组学生按照课本实验要求,用50mL0.5mol?L-1盐酸与50mL0.55mol?L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量计算中和热.下列说法正确的是( )| A、实验过程中没有热量损失 |
| B、图中实验装置缺少环形玻璃搅拌棒 |
| C、烧杯间填满碎泡沫塑料的作用是固定小烧杯 |
| D、酸或碱的物质的量越大,所测中和热的数值越大 |


