题目内容
10.下列说法错误的是( )| A. | 0.1 mol/L CH3COOH溶液中:c(CH3COO-)+c(CH3COOH)=0.1mol/L | |
| B. | 将Al2(SO4)3溶液蒸干,灼烧得Al2O3 | |
| C. | 配制FeCl3溶液,应加少量盐酸 | |
| D. | Na2S溶液中:c(OH-)═c(H+)+c(HS-)+2c(H2S) |
分析 A、根据物料守恒来分析;
B、硫酸铝水解为硫酸和氢氧化铝;
C、配制氯化铁溶液要抑制水解;
D、根据质子守恒来分析.
解答 解:A、醋酸是弱酸,在溶液中部分电离,根据物料守恒可知,c(CH3COO-)+c(CH3COOH)=0.1mol/L,故A正确;
B、硫酸铝水解为硫酸和氢氧化铝,将溶液蒸干时,硫酸不挥发,故水解不能彻底,蒸干灼烧后得到的仍为硫酸铝,故B错误;
C、配制氯化铁溶液要抑制水解,故在配制氯化铁溶液时应加盐酸来抑制水解,故C正确;
D、在硫化钠溶液中,硫离子会水解,将水电离出的部分氢离子结合,而水电离出的氢氧根个数等于氢离子的个数,根据质子守恒可知c(OH-)═c(H+)+c(HS-)+2c(H2S),故D正确.
故选B.
点评 本题考查了酸、盐溶液中的物料守恒、质子守恒和盐类水解的应用,难度不大,注意基础的掌握.

练习册系列答案
相关题目
20.有机物A的分子式为C5H12O2,则符合下列条件的有机化合物A的同分异物体有(不考虑立体异构)( )
①1molA可与金属钠反应放出1mol氢气 ②含2个-CH3 ③1个碳原子上不能连接2个羟基.
①1molA可与金属钠反应放出1mol氢气 ②含2个-CH3 ③1个碳原子上不能连接2个羟基.
| A. | 7种 | B. | 6种 | C. | 5种 | D. | 4种 |
1.下列物质的每步转化在给定条件下能一步实现的是( )
| A. | Fe$→_{点燃}^{O_{2}}$Fe2O3$\stackrel{H_{2}SO_{4}}{→}$Fe2(SO4)3 | |
| B. | 饱和食盐水$\stackrel{NH_{3},CO_{2}}{→}$NaHCO3$\stackrel{△}{→}$Na2CO3 | |
| C. | 海水$\stackrel{熟石灰}{→}$Mg(OH)2$\stackrel{△}{→}$MgO$\stackrel{电解}{→}$Mg | |
| D. | NH3$→_{催化剂,△}^{O_{2}}$N2$\stackrel{H_{2}O+O_{2}}{→}$HNO3 |
18.下列除杂方法不正确的是( )
| A. | 除去乙炔中混有的少量H2S气体:可用CuSO4溶液洗气 | |
| B. | 除去乙醛中混有的少量乙酸:可向混合物中加入足量的稀NaOH溶液,然后分液 | |
| C. | 除去苯中少量的苯酚:可向混合物中加入足量的浓溴水,过滤 | |
| D. | 除去溴苯中混有的少量液溴:可向混合物中加入足量的稀NaOH溶液,然后分液 |
15.下列有关化学键的叙述,不正确的是( )
| A. | 非金属元素构成的单质中一定存在共价键 | |
| B. | 由不同种原子间形成的共价键不一定是极性键 | |
| C. | 含有共价键的化合物不一定是共价化合物 | |
| D. | 化学键断裂,不一定发生化学变化 |
19.提出元素周期律并绘制了第一张元素周期表的化学家是( )
| A. | 戴维 | B. | 侯德榜 | C. | 门捷列夫 | D. | 道尔顿 |
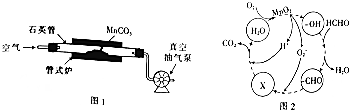
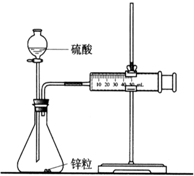 某化学兴趣小组的甲、乙两位同学对测定化学反应速率非常感兴趣,为此进行了有关的实验探究,实验记录如下.
某化学兴趣小组的甲、乙两位同学对测定化学反应速率非常感兴趣,为此进行了有关的实验探究,实验记录如下.