��Ŀ����
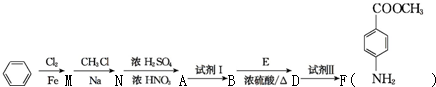
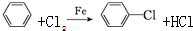
18�������ɱݣ�A����һ���µĿ��������֢ҩ����ɻ�����B��C��D���л��ܼ���ͨ����ͼ����·�ߺϳɵõ���
��·һ��B$��_{K_{2}CO_{3}}^{C}$E$��_{BaCO_{3}}^{D}$A
��·����C$��_{BaCO_{3}}^{D}$F$��_{K_{2}CO_{3}}^{B}$A
��1��E�Ľṹ��ʽΪ
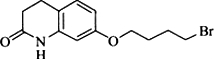 ���京�����������ļ����Ѽ���д���ƣ���
���京�����������ļ����Ѽ���д���ƣ�����2����C��D���ɻ�����F�ķ�Ӧ������ȡ����Ӧ��������C��������NaOH�Ҵ���Һ���ȷ�Ӧ�IJ����������1��3-����ϩ
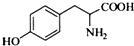
��3��H���ڰ����ᣬ��B��ˮ����ﻥΪͬ���칹�壮H����FeCl3��Һ������ɫ��Ӧ���ұ����ϵ�һ�ȴ���ֻ��2�֣�д��������������������H�Ľṹ��ʽ��
 ��
��
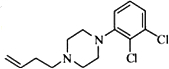
��4���ϳ�F����Է�������Ϊ366��ʱ����������һ����Է�������Ϊ285�ĸ�����G��G��ʹ��ˮ��ɫ��G�Ľṹ��ʽΪ
��5����֪��R-CHO$��_{��2��H_{3}O+}^{��1��HCN}$
 д����C�Ʊ�������
д����C�Ʊ������� �ĺϳ�·������ͼ�����Լ���ѡ�����ϳ�·������ͼʾ�����£�CH3CH2OH$��_{170��}^{Ũ����}$H2C$\stackrel{Br_{2}}{��}$
�ĺϳ�·������ͼ�����Լ���ѡ�����ϳ�·������ͼʾ�����£�CH3CH2OH$��_{170��}^{Ũ����}$H2C$\stackrel{Br_{2}}{��}$
���� ��1����A�Ľṹ��ʽ��֪��D��E����ȡ����Ӧ����A����EӦΪ ��
��
��2��F��B��Ӧ�õ�A���Ա�A��B�Ľṹ��֪FΪ ����C��D�ϳ����ɻ�����F��±��ԭ����H��ȡ����Ӧ��������C��������NaOH�Ҵ���Һ���ȷ�Ӧ�IJ���ΪCH2=CH-CH=CH2��
����C��D�ϳ����ɻ�����F��±��ԭ����H��ȡ����Ӧ��������C��������NaOH�Ҵ���Һ���ȷ�Ӧ�IJ���ΪCH2=CH-CH=CH2��
��3��H���ڰ����ᣬ��B��ˮ����ﻥΪͬ���칹�壮H����FeCl3��Һ������ɫ��Ӧ��˵�����з��ǻ����ұ����ϵ�һ�ȴ���ֻ��2�֣�˵��H�ķ����б�������������ͬȡ�����Ҵ��ڶ�λ��
��4��FΪ ����Է�������Ϊ366����G����Է�������285��ȣ�G��F�ٵ���Է��������൱��HBr�ģ����˷���ȡ����Ӧ�⣬����������ȥ��Ӧ��
����Է�������Ϊ366����G����Է�������285��ȣ�G��F�ٵ���Է��������൱��HBr�ģ����˷���ȡ����Ӧ�⣬����������ȥ��Ӧ��
��5��������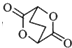 ���2������������
�к���2������������ ����������Ӧ��ȡ�����������Ϣ��֪
����������Ӧ��ȡ�����������Ϣ��֪ ����
���� ��HCN�ȼӳɡ���ˮ����ȡ����
��HCN�ȼӳɡ���ˮ����ȡ���� ����
���� ������������ȡ��
������������ȡ�� ����C����ȡ����Ӧ��ȡ��
����C����ȡ����Ӧ��ȡ��
��� �⣺��1����A�Ľṹ��ʽ��֪��D��E����ȡ����Ӧ����A����EӦΪ �����еĺ����������У��ļ����Ѽ���
�����еĺ����������У��ļ����Ѽ���
�ʴ�Ϊ�� ���ļ����Ѽ���
���ļ����Ѽ���
��2��F��B��Ӧ�õ�A���Ա�A��B�Ľṹ��֪FΪ ����C��D�ϳ����ɻ�����F��±��ԭ����H��ȡ����Ӧ��������C��������NaOH�Ҵ���Һ���ȷ�Ӧ�IJ���ΪCH2=CH-CH=CH2������Ϊ1��3-����ϩ��
����C��D�ϳ����ɻ�����F��±��ԭ����H��ȡ����Ӧ��������C��������NaOH�Ҵ���Һ���ȷ�Ӧ�IJ���ΪCH2=CH-CH=CH2������Ϊ1��3-����ϩ��
�ʴ�Ϊ��ȡ����Ӧ��1��3-����ϩ��
��3��H���ڰ����ᣬ��B��ˮ����ﻥΪͬ���칹�壮H����FeCl3��Һ������ɫ��Ӧ��˵�����з��ǻ����ұ����ϵ�һ�ȴ���ֻ��2�֣�˵��H�ķ����б�������������ͬȡ�����Ҵ��ڶ�λ������������H�Ľṹ��ʽΪ�� ��
�� ��
��
�ʴ�Ϊ�� ��
�� ��
��
��4��FΪ ����Է�������Ϊ366����G����Է�������285��ȣ�G��F�ٵ���Է��������൱��HBr�ģ����˷���ȡ����Ӧ�⣬����������ȥ��Ӧ����G�Ľṹ��ʽΪ��
����Է�������Ϊ366����G����Է�������285��ȣ�G��F�ٵ���Է��������൱��HBr�ģ����˷���ȡ����Ӧ�⣬����������ȥ��Ӧ����G�Ľṹ��ʽΪ�� ��
��
�ʴ�Ϊ�� ��
��
��5�������� ���2������������
�к���2������������ ����������Ӧ��ȡ�����������Ϣ��֪
����������Ӧ��ȡ�����������Ϣ��֪ ����
���� ��HCN�ȼӳɡ���ˮ����ȡ����
��HCN�ȼӳɡ���ˮ����ȡ���� ����
���� ������������ȡ��
������������ȡ�� ����C����ȡ����Ӧ��ȡ����ϳ�·������ͼΪ��
����C����ȡ����Ӧ��ȡ����ϳ�·������ͼΪ��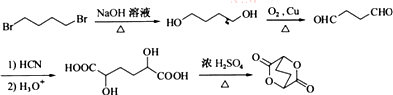 ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л�����ƶ���ϳɡ������Žṹ�����ʣ���������ͬ���칹����д���л���Ӧ���͵ȣ���һ���ۺ��Ե��л��ϳ����⣬���ؿ���ѧ���ķ�������������֪ʶǨ��������������Ŀ�ѶȽϴ�

| A�� | ���м���Ũ��ˮ�����ۣ����ȣ��ټ���AgNO3��Һ������������˵������Ũ��ˮ������ȡ����Ӧ | |
| B�� | ʵ�����Ʊ�����Ȳ����ͨ������һ���Ĵ̼�����ζ������ͨ��NaOH��Һ��Ũ����ϴ������ô�������Ȳ | |
| C�� | ��2%��AgNO3��Һ����εμ�2%�İ�ˮ��ֱ�������İ�ɫ����ǡ����ʧ�������Ƶõ�������Һ | |
| D�� | ��NaOH��Һ�м��������飬���ȣ��ټ���AgNO3��Һ������������˵�������鷢����ˮ�ⷴӦ |
| A�� | ��Ca��ClO��2��Һ��ͨ������SO2Ca2++3ClO-+SO2+H2O�TCaSO4��+Cl-+2HClO | |
| B�� | 1mol/L��NaAlO2��Һ��2.5mol/L�������������Ȼ�ϣ�2AlO2-+5H+�TAl��OH��3��+Al3++H2O | |
| C�� | ��11.2L��״���µ�����ͨ��200mL2mol/L��FeBr2��Һ�У����ӷ�Ӧ����ʽΪ��2Fe2++8Br-+5Cl2�T2Fe3++4Br2+10Cl- | |
| D�� | ��NH4HCO3��Һ�м�������NaAlO2��Һ��NH4++2AlO2-+HCO3--+2H2O�TNH3��+2Al��OH��3��+CO32-�� |
| A�� | v��O2��=0.01 mol/��L•s�� | B�� | v��NO��=0.08 mol/��L•s�� | ||
| C�� | v��H2O��=0.003 mol/��L•s�� | D�� | v��NH3��=0.001 mol/��L•s�� |
| ���� | �۵�/�� | �е�/�� | �������� |
| SO2Cl2 | -54.1 | 69.1 | ����ˮ�⣬������������ ���ֽ⣺SO2Cl2$\frac{\underline{\;100��\;}}{\;}$ SO2��+Cl2�� |
| H2SO4 | 10.4 | 338 | ��ˮ���Ҳ��ֽ� |

��1������A��ȴˮ�Ľ�ˮ��Ϊa���a����b������
��2������B��ʢ�ŵ�ҩƷ�Ǽ�ʯ�ң�
��3��ʵ��ʱ��װ�ö��з�����Ӧ�����ӷ���ʽΪClO3-+5Cl-+6H+=3Cl2��+3H2O��
��4��װ�ñ�������Ϊ��ȥCl2�е�HCl����ȱ��װ���ң��������Ȼ�ˮ�⣬�÷�Ӧ�Ļ�ѧ����ʽΪSO2Cl2+2H2O�TH2SO4+2HCl��
��5������������Ҳ�����Ȼ��ᣨClSO3H���ֽ��ã��÷�Ӧ�Ļ�ѧ����ʽΪ��2ClSO3H�TH2SO4+SO2Cl2���˷����õ��IJ�Ʒ�л�������ᣮ
�ٴӷֽ�����з���������ȵķ���������
�������ʵ�鷽�������Ʒ�������ᣨ��ѡ�Լ���ϡ���ᡢϡ���ᡢBaCl2��Һ������ˮ��ʯ����Һ����ȡ�����ڸ��������¼�������ȫ��Ӧ����ӷ���ֽ�ȣ�����ȴ���ˮϡ�ͣ�ȡ������Һ�μ���ɫʯ����Һ��죻��ȡ������Һ������BaCl2��Һ������ɫ������˵������H2SO4����ȡ��Ӧ��IJ���ֱ�Ӽ�BCl2��Һ���а�ɫ�������ٵμ���ɫʯ����Һ��죬˵������H2SO4��
 �����������ԣ���������
�����������ԣ���������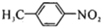 ��
��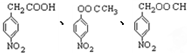 ����2�֣�
����2�֣�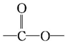 �ṹ��
�ṹ��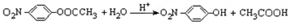 ��
��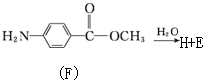 ������H��һ�������¾����۷�Ӧ���Ƶø߷�����ά���㷺����ͨѶ�����������������д�������۷�Ӧ�Ļ�ѧ����ʽ
������H��һ�������¾����۷�Ӧ���Ƶø߷�����ά���㷺����ͨѶ�����������������д�������۷�Ӧ�Ļ�ѧ����ʽ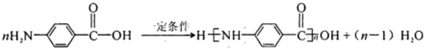 ��
��
 ά����K4�Ǻ������ɳɷ֣������ڲ���RNA��DNA�ϳɣ����������������������ƻ���Ƶ�����İ�ϸ�����٣������й�ά����K4˵����ȷ���ǣ�������
ά����K4�Ǻ������ɳɷ֣������ڲ���RNA��DNA�ϳɣ����������������������ƻ���Ƶ�����İ�ϸ�����٣������й�ά����K4˵����ȷ���ǣ�������