题目内容
9.下列有关实验叙述正确的是( )| A. | 向苯中加入浓溴水和铁粉,加热,再加入AgNO3溶液,产生沉淀,说明苯和浓溴水发生了取代反应 | |
| B. | 实验室制备的乙炔气体通常具有一定的刺激性气味,依次通过NaOH溶液、浓硫酸洗气,获得纯净的乙炔 | |
| C. | 向2%的AgNO3溶液中逐滴滴加2%的氨水,直至产生的白色沉淀恰好消失,即配制得到银氨溶液 | |
| D. | 向NaOH溶液中加入溴乙烷,加热,再加入AgNO3溶液,产生沉淀,说明溴乙烷发生了水解反应 |
分析 A.溴水中含有溴离子,可与硝酸银反应;
B.乙炔可被浓硫酸氧化而变质;
C.配制硝酸银溶液时注意氨水不能过量;
D.可能生成AgOH沉淀.
解答 解:A.苯和溴水不反应,溴水中含有溴离子,可与硝酸银反应生成沉淀,不能证明,故A错误;
B.乙炔可被浓硫酸氧化而变质,可用浓磷酸或碱石灰干燥,故B错误;
C.配制硝酸银溶液时注意氨水不能过量,可向2%的AgNO3溶液中逐滴滴加2%的氨水,直至产生的白色沉淀恰好消失即可,故C正确;
D.溶液呈碱性,不一定生成溴化银沉淀,可能生成AgOH沉淀,应先酸化,故D错误.
故选C.
点评 本题考查元素化合物知识的综合理解和运用,侧重于物质的性质等实验方案的评价,注意把握相关物质的性质,为解答该类题目的关键,有利于学习良好的科学素养的培养,题目难度中等.

练习册系列答案
相关题目
17.碳酸钠的用途很广,可用做冶金、纺织、漂染等工业的基本原料.请根据题意回答下列问题:
Ⅰ.世界最早工业生产碳酸钠的方法是路布兰(N.Leblanc)法.其流程如下:
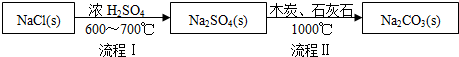
(1)流程I的另一产物是HCl,流程Ⅱ的反应分步进行:a.Na2SO4+4C $\frac{\underline{\;1000℃\;}}{\;}$ Na2S+4CO↑;
b.Na2S与石灰石发生复分解反应,总反应方程式可表示为Na2SO4+4C+CaCO3$\frac{\underline{\;1000℃\;}}{\;}$Na2CO3+CaS+4CO↑.
Ⅱ.1862年,比利时人索尔维(Ernest Solvay)用氨碱法生产碳酸钠.反应原理如下:
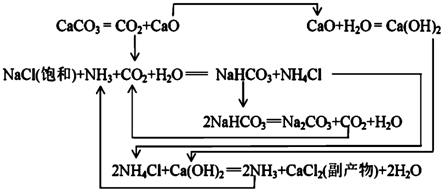
20℃时一些物质在水中的溶解度/g•(100gH2O)-1
(2)氨碱法生成纯碱的原料是食盐、石灰石、NH3,可循环利用的物质有CaO、CO2、NH4Cl、NH3.
(3)饱和NaCl溶液通NH3和CO2能生成NaHCO3的原因有:反应体系中NaHCO3溶解度最小,反应消耗水,NaHCO3相对分子质量最大.
Ⅲ.我国化工专家侯德榜研究出联合制碱法,其反应原理和氨碱法类似,但将制氨和制碱联合,提高了原料利用率.
(4)生产中需向分离出NaHCO3后所得的溶液中加入NaCl固体并通入NH3,在0~10℃(填温度范围)下析出NH4Cl.(填化学式)

Ⅰ.世界最早工业生产碳酸钠的方法是路布兰(N.Leblanc)法.其流程如下:
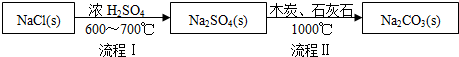
(1)流程I的另一产物是HCl,流程Ⅱ的反应分步进行:a.Na2SO4+4C $\frac{\underline{\;1000℃\;}}{\;}$ Na2S+4CO↑;
b.Na2S与石灰石发生复分解反应,总反应方程式可表示为Na2SO4+4C+CaCO3$\frac{\underline{\;1000℃\;}}{\;}$Na2CO3+CaS+4CO↑.
Ⅱ.1862年,比利时人索尔维(Ernest Solvay)用氨碱法生产碳酸钠.反应原理如下:

20℃时一些物质在水中的溶解度/g•(100gH2O)-1
| NaCl | NH4Cl | NaHCO3 | NH4HCO3 | Na2CO3 |
| 35.9 | 37.2 | 9.6 | 21.7 | 21.5 |
(3)饱和NaCl溶液通NH3和CO2能生成NaHCO3的原因有:反应体系中NaHCO3溶解度最小,反应消耗水,NaHCO3相对分子质量最大.
Ⅲ.我国化工专家侯德榜研究出联合制碱法,其反应原理和氨碱法类似,但将制氨和制碱联合,提高了原料利用率.
(4)生产中需向分离出NaHCO3后所得的溶液中加入NaCl固体并通入NH3,在0~10℃(填温度范围)下析出NH4Cl.(填化学式)

4.下列各组化合物中,化学键类型完全相同的是( )
| A. | CH4,H2O2,NH3 | B. | H2O,CO2,Na2O2 | C. | Na2O,NaCl,MgCl2 | D. | NaOH,NaClO,Na2O |
14.如图所示装置中,通电后可观察到Cu极溶解,下列说法正确的是( )
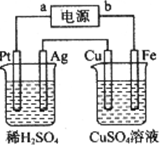

| A. | a极是直流电源的正极 | |
| B. | Fe极是阳极 | |
| C. | Pt极产生的气体体积是Ag极产生气体体积的2倍 | |
| D. | 硫酸铜溶液的浓度变大 |
1.下列有关物质的性质与应用均正确的是( )
| A. | Na2O2是碱性氧化物,具有强氧化性可用于杀菌消毒 | |
| B. | 乙烯能使溴水和酸性高锰酸钾溶液褪色,且褪色原理相同 | |
| C. | Mg(OH)2难溶于水,但可缓慢溶于浓的NH4Cl溶液 | |
| D. | 油脂在酸性条件下可以水解,可用此反应可以制作肥皂 |
19.设NA是阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4LNO和NH3的混合气体中,所含氮原子数为2NA | |
| B. | 1molFe粉与1mol水蒸气充分反应转移的电子数为3NA | |
| C. | 某温度下10LpH=11的NaOH溶液中含OH-的数目为NA,该温度下纯水的pH=6 | |
| D. | 含有阴、阳离子总数为1.5NA的NaHSO3溶液,浓度为0.5mol•L-1 |
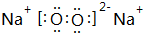 ;Z的化学式为SiO2.
;Z的化学式为SiO2.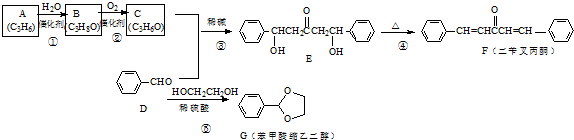
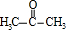 ;A加聚产物的结构简式是
;A加聚产物的结构简式是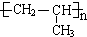 .
.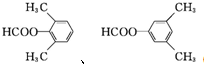 .
.
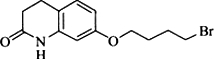 ,其含氧官能团有肽键、醚键(写名称).
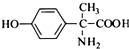
,其含氧官能团有肽键、醚键(写名称).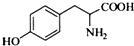 、
、
 写出由C制备化合物
写出由C制备化合物 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$H2C$\stackrel{Br_{2}}{→}$
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$H2C$\stackrel{Br_{2}}{→}$