题目内容
14.25℃时,实验室有浓度均为0.1mol•L-1的FeCl2溶液和AlCl溶液.(1)0.1mol•L-1的AlCl3溶液中c(OH-)•c(H+)=10-14.
(2)FeCl2溶液呈酸(填:“酸”“中”或“碱”)性,原因是Fe2++2H2O?Fe(OH)2+2H+(用离子方程式表示).
(3)把AlCl3溶液蒸干,灼烧,最后得到的固体产物主要是Al2O3.
分析 (1)25℃时,溶液中Kw=c(OH-)•c(H+);
(2)亚铁离子水解显酸性,其水解生成氢氧化亚铁和氢离子;
(3)氯化铝水解生成HCl和Al(OH)3,升高温度促进水解,Al(OH)3灼烧分解.
解答 解:(1)25℃时,溶液中Kw=c(OH-)•c(H+)=10-14;
故答案为:10-14;
(2)FeCl2为强酸弱碱盐,亚铁离子水解导致溶液呈酸性,水解方程式为Fe2++2H2O?Fe(OH)2+2H+;
故答案为:酸;Fe2++2H2O?Fe(OH)2+2H+;
(3)将AlCl3溶液蒸干过程中,氯化铝水解生成HCl和Al(OH)3,温度越高HCl挥发性越强,导致蒸干时得到的固体是Al(OH)3,灼烧Al(OH)3得到的固体是Al2O3;
故答案为:Al2O3.
点评 本题考查盐类水解,根据形成盐的酸、碱强弱确定盐的类型,从而确定溶液酸碱性,注意:蒸干、灼烧难挥发性酸的盐时得到盐本身,蒸干、灼烧挥发性酸的盐时得到金属氧化物.

练习册系列答案
相关题目
9.“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是( )
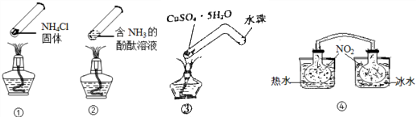

| A. | 加热时,①上部汇集了固体NH4Cl,说明NH4Cl易升华 | |
| B. | 加热时,②溶液颜色变,冷却后又恢复为原来的颜色 | |
| C. | 加热时,③中固体由蓝色变为白色,冷却后又恢复为原来的颜色 | |
| D. | ④中,浸泡在热水中的容器内气体颜色变深,说明受热时反应2NO2?N2O4向正方向移动 |

 水的电离程度与溶液中所溶解的电解质有关,如图是用一定浓度的盐酸滴定V mL同浓度的NH3•H2O时得到的滴定曲线.
水的电离程度与溶液中所溶解的电解质有关,如图是用一定浓度的盐酸滴定V mL同浓度的NH3•H2O时得到的滴定曲线. 将1molI2(g)和2molH2置于某2L密闭容器中,在一定温度下发生反应:
将1molI2(g)和2molH2置于某2L密闭容器中,在一定温度下发生反应: 工业上以黄铁矿为原料生产硫酸,其中重要的一步是催化氧化(生产中保持恒温恒容条件):2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ•mol-1
工业上以黄铁矿为原料生产硫酸,其中重要的一步是催化氧化(生产中保持恒温恒容条件):2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ•mol-1
 如图为实验室某浓盐酸试剂瓶标签上的有关数据u,试根据标签上的有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶标签上的有关数据u,试根据标签上的有关数据回答下列问题: