题目内容
9.某研究性学习小组选用以下装置进行实验设计和探究(图中a、b、c均为止水夹)
(1)在进行气体制备时,应先检验装置的气密性.将A装置末端导管密封后,在A装置的分液斗内装一定量的蒸馏水,然后打开分液漏斗开关,水不能顺利流下,则气密性良好或打开分液漏斗开关水不能持续滴下或分液漏斗中液面长期保持不变,则证明A装置的气密性良好.
(2)用锌粒和稀硫酸制备H2时应选用装置B作为发生装置(填所选装置的序号字母),夹紧止水夹后反应会慢慢停止下来,请描述原因试管中气压增大,将溶液压回长颈漏斗中,使固液分离而停止.
(3)某同学利用上述装置设计实验证明Cl2氧化性强于Br2
①选用的装置连接顺序为:A→C→E(填所选装置的序号字母);
②从以下试剂中选用该实验所需的试剂为b、c、e(填试剂的序号字母);
a.浓硫酸 b.浓盐酸 c.二氧化锰 d.氯化钠 e.溴化钠溶液
③实验过程中能说明Cl2氧化性强于Br2的实验现象是C中溶液的颜色变为(橙)黄色;
(4)另一同学将B、D、E装置连接后,在B装置中加入铜片和浓硝酸制取NO2,然后进行NO2气体与水反应的实验,并观察相关现象:
①B装置发生反应的离子方程式为Cu+4H++2NO3-=Cu2++2NO2↑+2H2O;
②反应一段时间后D装置中的具支试管乙中收集满NO2气体,若进行NO2气体与水反应的实验,应关闭止水夹a、b,打开止水夹c(填“对a、b、c三个止水夹进行的操作”),然后再适当加热乙,实验现象为烧杯中的水进入试管中,试管中气体颜色变浅.
分析 (1)将A装置末端导管密封后,在A装置的分液斗内装一定量的蒸馏水,利用气体的压强检验气密性;
(2)用锌粒和稀硫酸制备H2,选择固体与液体反应装置,且不需要加热;夹紧止水夹后反应会慢慢停止下来,气体使固液分离;
(3)设计实验证明Cl2氧化性强于Br2,利用A装置制备氯气,C装置发生氯气与NaBr的反应,E装置尾气处理;
(4)将B、D、E装置连接后,在B装置中加入铜片和浓硝酸制取NO2,然后进行NO2气体与水反应的实验,B中Cu与浓硝酸反应生成硝酸铜、二氧化氮和水,D装置中的具支试管乙中收集满NO2气体,关闭止水夹a、b,打开止水夹c,适当加热试管乙,可使二氧化氮与水反应生成NO,以此来解答.
解答 解:(1)在进行气体制备时,应先检验装置的气密性.将A装置末端导管密封后,在A装置的分液斗内装一定量的蒸馏水,然后打开分液漏斗开关,水不能顺利流下,则气密性良好或打开分液漏斗开关水不能持续滴下或分液漏斗中液面长期保持不变,则气密性良好,
故答案为:打开分液漏斗开关,水不能顺利流下,则气密性良好或打开分液漏斗开关水不能持续滴下或分液漏斗中液面长期保持不变;
(2)用锌粒和稀硫酸制备H2,选择固体与液体反应装置,且不需要加热,则选择装置B;夹紧止水夹后反应会慢慢停止下来,原因为试管中气压增大,将溶液压回长颈漏斗中,使固液分离而停止,
故答案为:B;试管中气压增大,将溶液压回长颈漏斗中,使固液分离而停止;
(3)设计实验证明Cl2氧化性强于Br2,利用A装置制备氯气,C装置发生氯气与NaBr的反应,E装置尾气处理,
①由上述分析可知,连接顺序为A→C→E,故答案为:A;C;E;
②利用浓盐酸与二氧化锰制备氯气,C中试剂为NaBr,即该实验需要的试剂为b、c、e,故答案为:b、c、e;
③实验过程中能说明Cl2氧化性强于Br2的实验现象是C中溶液的颜色变为(橙)黄色,故答案为:C中溶液的颜色变为(橙)黄色;
(4)①B中Cu与浓硝酸反应生成硝酸铜、二氧化氮和水,离子反应为Cu+4H++2NO3-=Cu2++2NO2↑+2H2O,
故答案为:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O;
②反应一段时间后D装置中的具支试管乙中收集满NO2气体,若进行NO2气体与水反应的实验,应关闭止水夹a、b,打开止水夹c,然后再适当加热乙,实验现象为烧杯中的水进入试管中,试管中气体颜色变浅,
故答案为:关闭止水夹a、b,打开止水夹c;乙;烧杯中的水进入试管中,试管中气体颜色变浅.
点评 本题考查性质实验方案的设计,为高频考点,把握常见气体的制备原理、性质实验设计、实验装置的作用为解答的关键,侧重分析与实验能力的考查,题目难度不大.

 考前必练系列答案
考前必练系列答案| A. | 10mol和10% | B. | 20mol和40% | C. | 20mol和20% | D. | 30mol和80% |
| A. | 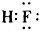 | B. | 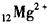 | C. |  | D. | OH- |
| A. | 若x>z则a>b | B. | x=y>z 则a<b | C. | x=z<y则a=b | D. | x<z=y则a<b |
 )是最常用的非甾体消炎解热镇痛药,可用如下方法合成:
)是最常用的非甾体消炎解热镇痛药,可用如下方法合成:

 .
.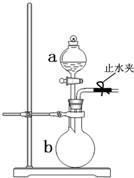 如图所示装置是实验室常用的气体制取装置.据图回答下列问题:
如图所示装置是实验室常用的气体制取装置.据图回答下列问题: