题目内容
20.除去物质中的杂质选用的试剂或操作方法,正确的是( )| 物质 | 杂质 | 除杂试剂或操作方法 | |
| A. | NaNO3 | CaCO3 | 溶解、过滤、蒸发 |
| B. | FeSO4 | CuSO4 | 加入NaOH溶液,过滤 |
| C. | NaCl溶液 | I2 | 加酒精,萃取分液 |
| D. | KNO3溶液 | AgNO3 | 加入NaCl溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.碳酸钙不溶于水,硝酸钠溶于水;
B.二者均与NaOH反应生成沉淀;
C.酒精与水不分层;
D.硝酸银与NaCl反应生成沉淀和NaCl.
解答 解:A.碳酸钙不溶于水,硝酸钠溶于水,则溶解、过滤、蒸发可分离,故A正确;
B.二者均与NaOH反应生成沉淀,不能除杂,应加足量铁粉、过滤,故B错误;
C.酒精与水不分层,应加四氯化碳、萃取分液,故C错误;
D.硝酸银与NaCl反应生成沉淀和NaCl,引入新杂质NaCl,应加KCl、过滤,故D错误;
故选A.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及发生的反应为解答的关键,注意元素化合物知识的综合应用,题目难度不大.

练习册系列答案
相关题目
9.设NA为阿伏伽德罗常数的值,下列叙述不正确的是( )
| A. | 1molNa与O2完全反应生成Na2O2和Na2O的混合物,转移电子的总数为NA | |
| B. | 室温下,31.0g白磷中含有的共价键数目为1.5NA | |
| C. | 常温常压下,17g甲基(-14CH3)含有的电子数为9NA | |
| D. | 常温下,1.0L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA |
8.钛被称为“第三金属”,其制取原料为金红石(TiO2),制取步骤为:
TiO2-→TiCl4$\stackrel{酶/800℃/Ar}{→}$Ti
已知:①C(s)+O2(g)═CO2(g)△H1
②2CO(g)+O2(g)═2CO2(g)△H2
③TiO2(s)+2Cl2(g)═TiCl4(s)+O2(g)△H3
则反应TiO2(s)+2Cl2(g)+2C(s)═TiCl4(s)+2CO(g)的△H为( )
TiO2-→TiCl4$\stackrel{酶/800℃/Ar}{→}$Ti
已知:①C(s)+O2(g)═CO2(g)△H1
②2CO(g)+O2(g)═2CO2(g)△H2
③TiO2(s)+2Cl2(g)═TiCl4(s)+O2(g)△H3
则反应TiO2(s)+2Cl2(g)+2C(s)═TiCl4(s)+2CO(g)的△H为( )
| A. | △H3+2△H1+2△H2 | B. | △H3+2△H1+△H2 | C. | △H3+2△H1-△H2 | D. | △H3+2△H1-2△H2 |
15.将一定质量的钠铝合金置于水中,合金全部溶解.得到20mLNaOH和NaAlO2的混合溶液,然后用lmol/L的盐酸与之反应.至沉淀量最大时消耗盐酸40mL,则原合金中钠的质量为( )
| A. | 0.92g | B. | 0.69g | C. | 0.46g | D. | 0.23g |
5.在1L的密闭容器中通入2molNH3,在一定温度下发生下列反应:2NH3?N2+3H2,达到平衡时,容器内N2的百分含量为a%.若维持容器的体积和温度都不变,分别通入下列初始物质,达到平衡时,容器内N2的百分含量也为a%的是( )
| A. | 3molH2+2molN2 | B. | 2molNH3+1molN2 | ||
| C. | 3molN2+1molH2 | D. | 0.1molNH3+0.95molN2+2.85molH2 |
12.金属钛(Ti)被誉为21世纪金属,具有良好的生物相容性,它兼具铁的高强度和铝的低密度.其单质和化合物具有广泛的应用价值.氮化钛(Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金的代替品.以TiCl4为原料,经过一系列反应可以制得Ti3N4和纳米TiO2(如图1).
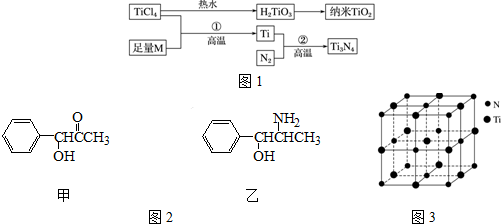
图中的M是短周期金属元素,M的部分电离能如表:请回答下列问题:
(1)Ti的基态原子外围电子排布式为4d25s2;
(2)M是Mg(填元素符号),该金属晶体的堆积模型为六方最密堆积,配位数为12;
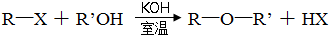
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如图2所示.化合物甲的分子中采取sp2方式杂化的碳原子有7个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为O>N>C;
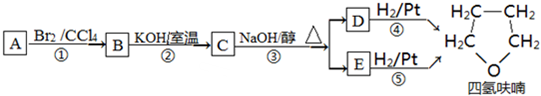
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图3所示,该晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为$\frac{4×62}{{N}_{A}×(2a×1{0}^{-10})^{3}}$ g•cm-3(NA为阿伏加德罗常数的值,只列计算式).该晶体中与N原子距离相等且最近的N原子有12个;
(5)科学家通过X-射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似.且知三种离子晶体的晶格能数据如下:
KCl、CaO、TiN三种离子晶体熔点由高到低的顺序为TiN>CaO>KCl.

图中的M是短周期金属元素,M的部分电离能如表:请回答下列问题:
| I1 | I2 | I3 | I4 | I5 | |
| 电离能/kJ•mol-1 | 738 | 1451 | 7733 | 1054 0 | 13630 |
(2)M是Mg(填元素符号),该金属晶体的堆积模型为六方最密堆积,配位数为12;
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如图2所示.化合物甲的分子中采取sp2方式杂化的碳原子有7个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为O>N>C;
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图3所示,该晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为$\frac{4×62}{{N}_{A}×(2a×1{0}^{-10})^{3}}$ g•cm-3(NA为阿伏加德罗常数的值,只列计算式).该晶体中与N原子距离相等且最近的N原子有12个;
(5)科学家通过X-射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似.且知三种离子晶体的晶格能数据如下:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3401 |
9.某化学兴趣小组欲研究一种镁铝合金,以下是部分实验.请完成填空.
[实验一]从镁铝合金片上剪下一小块,先称重,然后投到盛有10mL 10mol•L-1NaOH溶液(足量)的锥形瓶里.
(1)从反应开始至反应结束,依次可观察到的现象有:①切口断面处先产生气泡,反应由慢到快;②小块合金在溶液中上下翻腾;③溶液升温;④反应后,溶液中残留黑色固体.
(2)开始时产生气泡速率慢,其主要原因(除温度、电化学因素外)是合金表面有氧化膜.
(3)欲利用此反应测定合金中铝的含量,请仿照方法①写出另一种不同方法所需数据.
[实验二]向实验一的锥形瓶里滴加1mol•L-1HCl,使镁、铝两种元素恰好只以氯化物的形式存在.
[实验三]请设计合理实验检验实验二所得溶液中的Mg2+、Al3+.
限选实验用品与试剂:烧杯、试管、滴管、1mol•L-1NaOH溶液、1mol•L-1HCl溶液、蒸馏水.
根据你设计的实验方案,叙述实验操作、预期现象和结论.(可填满、可不填满)
[实验四]粉末状试样A是由MgO和Fe2O3组成的混合物.取适量A进行铝热反应,产物中有单质B生成.
产物中的单质B是Fe(填化学式).
[实验一]从镁铝合金片上剪下一小块,先称重,然后投到盛有10mL 10mol•L-1NaOH溶液(足量)的锥形瓶里.
(1)从反应开始至反应结束,依次可观察到的现象有:①切口断面处先产生气泡,反应由慢到快;②小块合金在溶液中上下翻腾;③溶液升温;④反应后,溶液中残留黑色固体.
(2)开始时产生气泡速率慢,其主要原因(除温度、电化学因素外)是合金表面有氧化膜.
(3)欲利用此反应测定合金中铝的含量,请仿照方法①写出另一种不同方法所需数据.
| 方法 | 需测定的数据 |
| ① | 测定产生的H2的体积 |
| ② | “测定残留固体镁的质量”或“测定反应消耗或剩余的NaOH的量”或“测定生成的NaAlO2的量” |
[实验三]请设计合理实验检验实验二所得溶液中的Mg2+、Al3+.
限选实验用品与试剂:烧杯、试管、滴管、1mol•L-1NaOH溶液、1mol•L-1HCl溶液、蒸馏水.
根据你设计的实验方案,叙述实验操作、预期现象和结论.(可填满、可不填满)
| 实验操作 | 预期现象和结论 |
| 步骤1: | |
| 步骤2: | |
| … |
产物中的单质B是Fe(填化学式).
 ,
,
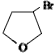 ,D
,D ,E
,E .
. .
.