题目内容
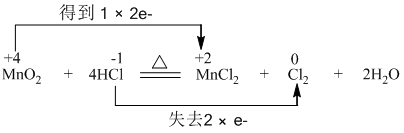
8.硫的化合价很多.已知硫与氢氧化钾发生如下反应.3S+6KOH═2K2S+1K2SO3+3H2O
①请配平上述化学方程式[3分]并标出电子转移的方向和数目.
②若有6mol电子发生转移,则作氧化剂的S为3mol.
③K2SO3属于离子化合物[填“离子化合物”或“共价化合物”];该化合物中含有的化学键有:离子键和共价键; K2SO3溶液露置空气中很容易变质,其主要原因是:K2SO3(或SO32-)原性强易被空所中的氧气氧化而变质.
分析 ①分析反应中各元素化合价变化,所含元素化合价升高为还原剂,所含元素化合价降低的为氧化剂,依据得失电子数目相等、原子个数守恒配平方程式,用双线桥表示电子转移方向和数目;
②依据①电子转移数目计算氧化剂的物质的量;
③亚硫酸钾中钾离子与亚硫酸根离子通过离子键结合,氧原子与硫原子通过共价键结合,据此判断化合物类型;
依据亚硫酸钾中硫的化合价判断亚硫酸钾性质,据此解答K2SO3溶液露置空气中很容易变质原因.
解答 解:①方程式中:硫元素部分化合价从0升高为+4价,部分从0降为-2价,所以硫既是氧化剂又是还原剂,要使得失电子守恒,则硫化钾系数为2,亚硫酸钾系数为1,依据原子个数守恒,方程式为:3S+6KOH═2K2S+1K2SO3+3H2O,用双线桥表示为: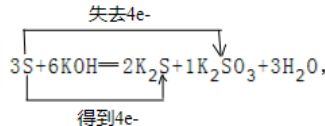 ;
;
故答案为:3;6;2;1;3; ;
;
②依据方程式:S(还原剂)+2S(氧化剂)+6KOH═2K2S+1K2SO3+3H2O~转移4mole-,可知若有6mol电子发生转移,则作氧化剂的S为3mol;
故答案为:3;
③亚硫酸钾中钾离子与亚硫酸根离子通过离子键结合,氧原子与硫原子通过共价键结合,所以亚硫酸钾既含有离子键又含有共价键,含有离子键的化合物为离子化合物,所以亚硫酸钾为离子化合物;亚硫酸钾中硫化合价为+4价,具有强的还原性,极易被空气中的氧气氧化,所以K2SO3溶液露置空气中很容易变质;
故答案为:离子化合物;离子键和共价键;K2SO3(或SO32-)还原性强易被空所中的氧气氧化而变质;
点评 本题考查了氧化还原反应及化学键,涉及氧化还原反应化学方程式的配平、双线桥表示方法、电子转移数目计算、化学键类型判断,题目难度不大,掌握基础是解题关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.下列叙述正确的是( )
| A. | 电子的能量越低,运动区域离核越远 | |
| B. | 当M层是最外层时,最多可排布18个电子 | |
| C. | 稀有气体元素原子的最外层都排有8个电子 | |
| D. | 核外电子的分层排布即是核外电子的分层运动 |
3.X、Y两种元素的原子序数之和为19,X在元素周期表中位于Y的上一周期,且X为非金属,Y为金属.则X、Y两种元素组成的化合物的化学式不正确的是( )
| A. | XY | B. | Y2X | C. | Y2X2 | D. | Y3X2 |
13.下列四种固体物质中,既存在离子键又存在共价键的是( )
| A. | NH4Cl | B. | HCl | C. | MgCl2 | D. | CH4 |
20.短周期元素X、Y、Z、W、Q在元素周期表中的位置如图所示,Z元素的简单离子半径在本周期中最小,下列说法不正确的是( )
| X | Y | |||
| z | W | Q |
| A. | Y元素气态氢化物的稳定性大于X元素的气态氢化物 | |
| B. | 形成的简单离子半径:W>Q>Z>X | |
| C. | Q的最高价氧化物对应的水化物酸性最强 | |
| D. | X的最高价氧化物对应的水化物与其氢化物形成的化合物中含有离子键和共价键 |
17.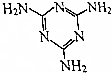 三聚氰胺的结构式如图所示,尿素[CO(NH2)2]在一定条件下发生分解反应可制得三聚氰胺和CO2等物质,下列说法不正确的是( )
三聚氰胺的结构式如图所示,尿素[CO(NH2)2]在一定条件下发生分解反应可制得三聚氰胺和CO2等物质,下列说法不正确的是( )
 三聚氰胺的结构式如图所示,尿素[CO(NH2)2]在一定条件下发生分解反应可制得三聚氰胺和CO2等物质,下列说法不正确的是( )
三聚氰胺的结构式如图所示,尿素[CO(NH2)2]在一定条件下发生分解反应可制得三聚氰胺和CO2等物质,下列说法不正确的是( )| A. | 三聚氰胺的分子式为C3H6N6 | |
| B. | 氰胺的结构简式为H2N-C≡N | |
| C. | 尿素分解制三聚氰胺时,除生成CO2外,还会生成NH3 | |
| D. | 三聚氰胺属于高分子化合物 |
20.除去物质中的杂质选用的试剂或操作方法,正确的是( )
| 物质 | 杂质 | 除杂试剂或操作方法 | |
| A. | NaNO3 | CaCO3 | 溶解、过滤、蒸发 |
| B. | FeSO4 | CuSO4 | 加入NaOH溶液,过滤 |
| C. | NaCl溶液 | I2 | 加酒精,萃取分液 |
| D. | KNO3溶液 | AgNO3 | 加入NaCl溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |