题目内容
18.下列各组中,互称为同素异形体的是( )| A. | O2与O3 | B. | 35Cl与37Cl | C. | 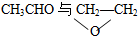 | D. | CH4与C2H6 |
分析 A.O2与O3分子式不相同,互为同素异形体;
B.35Cl和37Cl中子数不同,是氯元素的不同核素;
C.乙醛和环氧乙烷是分子式相同结构不同;
D.CH4与C2H6都属于烷烃中不同的化合物.
解答 解:A.O2与O3分子式不相同,形成元素相同,互为同素异形体,故A正确;
B.35Cl与37Cl中子数不同,是碳元素的不同核素,互为同位素,故B错误;
C.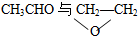 分子式相同,结构不同属于同分异构体,故C错误;
分子式相同,结构不同属于同分异构体,故C错误;
D.CH4与C2H6都属于烷烃中不同的化合物属于同系物,故D错误;
故选A.
点评 本题考查同素异形体,难度不大,同素异形体是指由同一种元素组成的不同单质,互为同素异形体.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
2.下列说法正确的是( )
| A. | 乙酸与NaHCO3反应生成CO2气体,说明乙酸的酸性强于碳酸 | |
| B. | 乙烯使溴水褪色的反应方程式是:CH2=CH2+Br2→CH3CHBr2 | |
| C. | 乙烯和苯分子中都存在碳碳双键,都能发生加成反应 | |
| D. | 乙醇能发生氧化反应,乙酸不能发生氧化反应 |
6.关于晶体的下列说法正确的是( )
| A. | 晶体中的化学键都具有饱和性和方向性 | |
| B. | 晶体中只要有阴离子,就一定有阳离子 | |
| C. | 石墨是一种典型的原子晶体 | |
| D. | 冰中存在极性共价键和氢键两种化学键 |
10.下列离子方程式中,正确的是( )
| A. | Ca(ClO)2溶液中通入过量的CO2:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO | |
| B. | 钠和冷水反应:Na+2H2O=Na++2OH-+H2↑ | |
| C. | 氯气和水反应:Cl2+H2O=2H++Cl-+ClO- | |
| D. | NaHCO3溶液与NaOH溶液反应:OH-+HCO3-=CO32-+H2O |
8.下列各组物质中,属于同素异形体的是( )
| A. | S2、S4 | B. | 碘晶体、碘蒸气 | ||
| C. | H、D | D. | ${\;}_{8}^{16}$O2、${\;}_{8}^{18}$O2 |
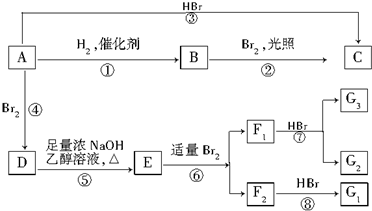
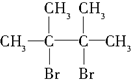 )(F1和F2互为同分异构体)(G1和G2互为同分异构体)
)(F1和F2互为同分异构体)(G1和G2互为同分异构体) .
. .
.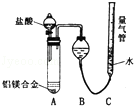 2011年初,我国“歼20”的试飞引起了世界各国的关注,为减轻飞机的重量,飞机常采用密度较小的镁铝合金作为飞机主体.工厂检测员常通过检测合金中各元素的含量确定合金是否合格.某研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其它元素)中镁的质量分数,设计了下列两种不同实验方案进行探究.填写下列空白.
2011年初,我国“歼20”的试飞引起了世界各国的关注,为减轻飞机的重量,飞机常采用密度较小的镁铝合金作为飞机主体.工厂检测员常通过检测合金中各元素的含量确定合金是否合格.某研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其它元素)中镁的质量分数,设计了下列两种不同实验方案进行探究.填写下列空白.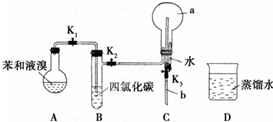
 ,烧瓶a中的实验现象是烧杯中的水沿玻璃管上升进入烧瓶,形成喷泉.
,烧瓶a中的实验现象是烧杯中的水沿玻璃管上升进入烧瓶,形成喷泉.