题目内容
3. 2011年初,我国“歼20”的试飞引起了世界各国的关注,为减轻飞机的重量,飞机常采用密度较小的镁铝合金作为飞机主体.工厂检测员常通过检测合金中各元素的含量确定合金是否合格.某研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其它元素)中镁的质量分数,设计了下列两种不同实验方案进行探究.填写下列空白.
2011年初,我国“歼20”的试飞引起了世界各国的关注,为减轻飞机的重量,飞机常采用密度较小的镁铝合金作为飞机主体.工厂检测员常通过检测合金中各元素的含量确定合金是否合格.某研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其它元素)中镁的质量分数,设计了下列两种不同实验方案进行探究.填写下列空白.实验方案I:铝镁合金$\stackrel{NaOH溶液}{→}$ 测定剩余固体质量
实验中发生反应的化学方程式是2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
实验步骤:
(1)称取5.4g铝镁合金粉末样品,投入VmL 2.0mol/L NaOH溶液中,充分反应.NaOH溶液的体积V≥97mL.
(2)过滤、洗涤、干燥、称量固体.该步骤中若未洗涤固体,测得镁的质量分数将偏高(填“偏高”或“偏低”).
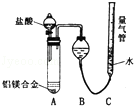
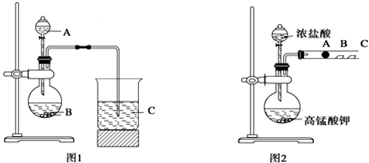
实验方案Ⅱ:铝镁合金$\stackrel{盐酸}{→}$测定生成气体的体积实验装置如图,问题讨论:
(3)某同学提出该实验装置不够完善,应在A、B之间添加一个干燥、除酸雾的装置.你的意见是:不需要(填“需要”或“不需要”).
(4)为使测定结果尽可能精确,实验中应注意的问题是(写出两点):①调整量气管C的高度,使C中液面与B液面相平;②待冷却至室温再读体积.
分析 镁铝合金和氢氧化钠溶液反应,铝溶解生成偏铝酸钠和氢气;
实验方案I:铝与氢氧化钠溶液反应生成偏铝酸钠与氢气;
(1)镁的质量分数最小时,金属铝的质量最大,需要的氢氧化钠溶液最多,实际需要氢氧化钠溶液的体积应大于或等于最大值,据此计算;
(2)镁上会附着偏铝酸钠等物质,未洗涤导致测定的镁的质量偏大;
实验方案Ⅱ:
(3)氯化氢极易溶于水,挥发的氯化氢不影响氢气体积的测定结果,所以不需要加除雾装置;
(4)调整量气管C的高度,使C中液面与B液面相平,待冷却至室温再读体积等会影响测定结果.
解答 解:实验方案I:铝与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(1)含镁为零时,金属铝的含量最高,5.4g合金中铝的质量为,5,4g×97%=5.238g,则:
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
54g 2mol
5.238g V×10-3L×2.0mol/L
所以54g:5.238g=2mol:(V×10-3L×2.0mol/L),
解得:V=97mL,故V(NaOH溶液)≥97mL;
故答案为:97mL;
(2)镁上会附着偏铝酸钠等物质,未洗涤导致测定的镁的质量偏大,镁的质量分数偏高,则铝的质量分数偏低,故答案为:偏高;
实验方案Ⅱ:
(3)由于氯化氢极易溶于水,挥发的氯化氢不影响氢气体积的测定结果,所以不需要加除雾装置,故答案为:不需要;
(4)调整量气管C的高度,使C中液面与B液面相平,待冷却至室温再读体积等会影响测定结果;
故答案为:调整量气管C的高度,使C中液面与B液面相平;待冷却至室温再读体积.
点评 本题考查物质含量的测定、对实验原理与装置的理解、实验方案设计等,难度中等,理解实验原理是解题的关键,是对知识的综合考查,需要学生具有知识的基础与综合运用知识分析问题、解决问题的能力.

 通城学典默写能手系列答案
通城学典默写能手系列答案主要成分:Al2O3杂质:Fe2O3、SiO2及其他不溶且不参与化学反应的物质为测定该样品中Al的含量,某化学兴趣小组设计了如下两个方案:
【查阅资料】各相关离子开始沉淀和沉淀完全时溶液的pH如表:
| Al3+ | Fe3+ | AlO2- | SiO32- | |
| 开始沉淀时 | 3.4 | 1.9 | 10.6 | 7.3 |
| 沉淀完全时 | 4.7 | 3.2 | 9.3 | 5.3 |
方案二:

(1)②反应的离子方程式为OH-+CO2=CO32-+H2O,2AlO2-+CO2+3H2O=CO32-+2Al(OH)3↓.CO2不可过量的原因是防止SiO32-被沉淀.
(2)若在步骤②中加入乙酸乙酯调节pH,加热也可得到d的沉淀,写出生成d沉淀的化学方程式AlO2-+CH3COOCH2CH3+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$CH3COO-+Al(OH)3↓+CH3CH2OH.
| A. | 褪色 | B. | 仍为紫色 | C. | 变红 | D. | 变蓝 |
| A. | O2与O3 | B. | 35Cl与37Cl | C. | 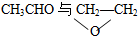 | D. | CH4与C2H6 |
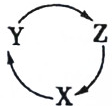 表中各组物质中,不能满足如图所示一步转化关系的是( )
表中各组物质中,不能满足如图所示一步转化关系的是( ) 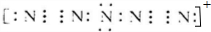 .
.
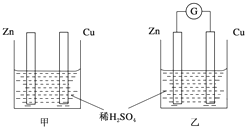 ①分别按图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计.请回答下列问题:
①分别按图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计.请回答下列问题: