题目内容
13.22克CO2的物质的量为0.5mol,含质子的物质的量为11mol,该气体在标准状况下的体积为11.2L.分析 根据n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$,结合物质的组成计算相关物理量.
解答 解:n(CO2)=$\frac{22g}{44g/mol}$=0.5mol,含质子的物质的量为0.5mol×(6+8×2)=11mol,该气体在标准状况下的体积为0.5mol×22.4L/mol=11.2L,
故答案为:0.5;11;11.2.
点评 本题考查物质的量的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握相关计算公式的运用以及物质的构成,难度不大.

练习册系列答案
相关题目
1.用容量瓶配制一定物质的量浓度的溶液,该容量瓶必须是( )
| A. | 干燥的 | B. | 瓶塞不漏水的 | ||
| C. | 用欲配制的溶液润洗过的 | D. | 以上三项均须要求的 |
8.几种短周期元素的原子半径及主要化合价如表,下列说法正确的是( )
| 元素代号 | X | Y | Z | M | R | Q | |
| 原子半径(×10-10m) | 0.37 | 1.86 | 1.43 | 0.99 | 0.75 | 0.74 | |
| 主要化合价 | 最高正价 | +1 | +1 | +3 | +7 | +5 | \ |
| 最低负价 | -1 | \ | \ | -1 | -3 | -2 | |
| A. | 元素X、Z、R的离子均能影响水的电离平衡 | |
| B. | Y、Z、M、R四种元素的最高价氧化物的水化物两两之间会发生反应 | |
| C. | 化合物XM、YM都是电解质,熔融状态下都能导电 | |
| D. | 离子半径大小:M>Y>Z>R |
18.在0.1mol•L-1的CH3COOH溶液中,要促进醋酸电离,且c(H+)增大,应采取的措施是( )
| A. | 加入等体积1mol/L的CH3COOH溶液 | B. | 升高温度 | ||
| C. | 加入NaOH溶液 | D. | 加入等体积0.1 mol•L-1 HCl |
5.能正确表示下列反应的离子方程式的是( )
| A. | 石灰石跟盐酸反应:CO32-+2H+═CO2↑+H2O | |
| B. | 氢氧化钡溶液与盐酸的反应OH-+H+═H2O | |
| C. | 铜片插入硝酸银溶液中Cu+Ag+═Cu2++Ag | |
| D. | 硫酸铜溶液和氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ |
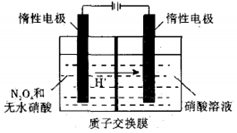 N2O5是绿色硝化试剂,溶于水可得硝酸.图是以N2O4为原料电解制备N2O5的装置示意图写出阳极区生成N2O5的电极反应式是N2O4-2e-+2HNO3=2N2O5+2H+.
N2O5是绿色硝化试剂,溶于水可得硝酸.图是以N2O4为原料电解制备N2O5的装置示意图写出阳极区生成N2O5的电极反应式是N2O4-2e-+2HNO3=2N2O5+2H+.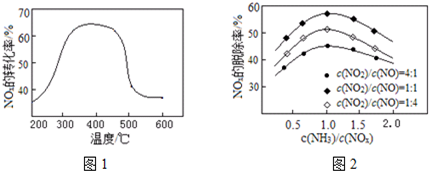
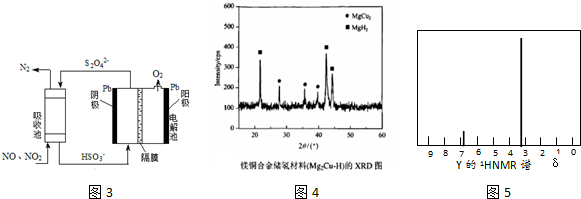
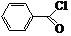 .
.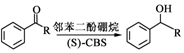 .
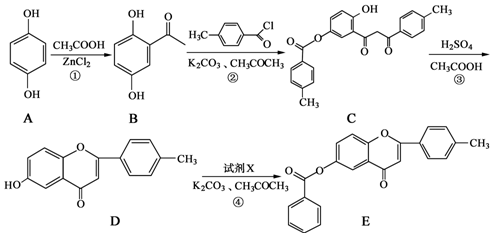
.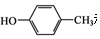 和CH3COOH为原料制备
和CH3COOH为原料制备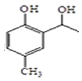 的合成路线流程图(无机试剂任选).
的合成路线流程图(无机试剂任选).