题目内容
18.在0.1mol•L-1的CH3COOH溶液中,要促进醋酸电离,且c(H+)增大,应采取的措施是( )| A. | 加入等体积1mol/L的CH3COOH溶液 | B. | 升高温度 | ||
| C. | 加入NaOH溶液 | D. | 加入等体积0.1 mol•L-1 HCl |
分析 根据题意知,要使平衡向正反应方向移动,加入的物质和醋酸电离出来的离子反应或升高温度,再结合氢离子的浓度变化分析.
解答 解:A.加入等体积1mol/L的CH3COOH溶液,醋酸的浓度增大,平衡正向移动,氢离子浓度增大,故A正确;
B.醋酸电离为吸热过程,升高温度,平衡向正反应方向移动,c(H+)增大,故B正确;
C.加入NaOH溶液,能促进醋酸的电离,但氢离子浓度减小,故C错误;
D.加入盐酸,增大c(H+),平衡逆向移动,故D错误;
故选AB.
点评 本题考查了影响弱电解质电离的因素,难度不大,注意:如果加入含有相同离子的物质就抑制其电离,如果加入和弱电解质电离的离子发生反应的物质就促进其电离.

练习册系列答案
相关题目
2.下列变化中,属于还原反应的是( )
| A. | KMnO4→MnO2 | B. | FeCl2→FeCl3 | C. | C→CO2 | D. | Cl-→Cl2 |
9.下列各组物质中,一定互为同系物的是( )
| A. | 淀粉和纤维素 | B. | 蔗糖和麦芽糖 | ||
| C. | 分子式为C4H6和C5H8的烃 | D. | 分子式为C4H10和C20H42的烃 |
3.对于溶液中的反应:2KMnO4+10FeSO4+8H2SO4═5Fe2(SO4)3+2MnSO4+K2SO4+8H2O,下列措施能使化学反应速率提高的是( )
| A. | 加水 | B. | 增加同浓度FeSO4的用量 | ||
| C. | 加压 | D. | 加入少量KMnO4晶体 |
7.使煤在煤炉中充分燃烧,一定可行的措施是( )
| A. | 把煤块制成煤球 | B. | 扩大煤炉的体积 | ||
| C. | 向炉内吹人适当过量的空气 | D. | 使用MnO2作催化剂 |
8.描述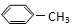 分子结构的下列叙述中,正确的是( )
分子结构的下列叙述中,正确的是( )
 分子结构的下列叙述中,正确的是( )
分子结构的下列叙述中,正确的是( )| A. | 七个碳原子可能不在同一平面上 | B. | 具有单键和双键两种键 | ||
| C. | 八个氢原子不可能都在同一平面上 | D. | 最多可能有5个C原子在一条直线上 |