题目内容
20. 某同学分析Zn 与稀H2SO4的反应.
某同学分析Zn 与稀H2SO4的反应.(1)该反应的离子方程式是Zn+2H+=Zn2++H2↑.
(2)制H2时,用稀硫酸而不用浓硫酸,原因是浓H2SO4具有强氧化性,不能生成氢气.
(3)已知:Zn(s)+$\frac{1}{2}$O2(g)═ZnO(s)△H=-332kJ/mol
ZnO(s)+H2SO4(aq)═ZnSO4(aq)+H2O(l)△H=-112kJ/mol
H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-286kJ/mol 则Zn 与稀H2SO4反应生成1mol H2时的反应热△H=kJ/mol.
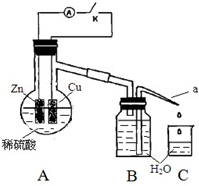
(4)该同学用如下装置进行实验,分析影响反应速率的因素.
实验时,从断开K 开始,每间隔1 分钟,交替断开或闭合K,并连续计数每1 分钟内从a 管流出的水滴数,得到的水滴数如下表所示:
| 1 分钟水滴数(断开K) | 34 | 59 | 86 | 117 | … | 102 |
| 1 分钟水滴数(闭合K) | 58 | 81 | 112 | 139 | … | 78 |
①由水滴数58>34、81>59,说明在反应初期,闭合K 时比断开K 时的反应速率快(填“快”或“慢”),主要原因是形成原电池反应速度快.
②由水滴数102>78,说明在反应后期,断开K 时的反应速率快于闭合K 时的反应速率,主要原因是断开K时,溶液中的c(H+)大于闭合K时溶液中的c(H+).
③从能量转换形式不同的角度,分析水滴数86>81、117>112 的主要原因是断开K时,反应的化学能主要转化成热能;闭合K时,反应的化学能主要转化成电能,前者使溶液的温度升得更高,故反应速率更快.
分析 (1)Zn与稀硫酸反应生成硫酸锌和氢气;
(2)浓硫酸具有强氧化性,与锌反应生成二氧化硫、硫酸锌、水;
(3)①Zn(s)+$\frac{1}{2}$O2(g)=ZnO(s)△H=-332kJ/mol
②ZnO(s)+H2SO4(aq)=ZnSO4(aq)+H2O(l)△H=-112kJ/mol
③H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-286kJ/mol
根据盖斯定律:①+②-③得Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2↑,据此计算;
(4)①形成原电池能加快反应速率;
②根据氢离子浓度大小与速率的关系分析;
③断开K时,反应的化学能主要转化成热能,闭合K时,反应的化学能主要转化成电能,根据温度对速率的影响分析
解答 解:(1)Zn与稀硫酸反应生成硫酸锌和氢气,其反应的离子方程式为:Zn+2H+=Zn2++H2↑;
故答案为:Zn+2H+=Zn2++H2↑;
(2)浓硫酸具有强氧化性,与锌反应生成二氧化硫、硫酸锌、水,不能生成氢气,稀硫酸才能与锌反应生成氢气;
故答案为:浓H2SO4具有强氧化性,不能生成氢气;
(3)①Zn(s)+$\frac{1}{2}$O2(g)=ZnO(s)△H=-332kJ/mol
②ZnO(s)+H2SO4(aq)=ZnSO4(aq)+H2O(l)△H=-112kJ/mol
③H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-286kJ/mol
根据盖斯定律:①+②-③得Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2↑,则△H=(-332kJ/mol)+(-112kJ/mol)-(-286kJ/mol)=-158kJ/mol;
故答案为:-158;
(4)①形成原电池能加快反应速率,所以在反应初期,闭合K时比断开K时的反应速率快,
故答案为:快;形成原电池反应速度快;
②由于反应前期形成原电池反应速率快,氢离子消耗的多,则在后期,闭合K时溶液中氢离子浓度小,氢离子浓度越小反应速率越小,断开K时,溶液中的c(H+)大于闭合K时溶液中的c(H+),所以在反应后期,断开K时的反应速率快于闭合K时的反应速率;
故答案为:断开K时,溶液中的c(H+)大于闭合K时溶液中的c(H+);
③断开K时,反应的化学能主要转化成热能,闭合K时,反应的化学能主要转化成电能,则随着反应进行,断开K时,放出的热量使溶液的温度升高,温度越高反应速率越快;
故答案为:断开K时,反应的化学能主要转化成热能,闭合K时,反应的化学能主要转化成电能,前者使溶液的温度升得更高,故反应速率更快.
点评 本题考查了盖斯定律的应用、原电池原理的应用、影响速率的因素等,题目难度中等,注意形成原电池能加快反应速率,侧重于考查学生的分析能力和对基础知识的应用能力.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | Na+、Al3+、Cl-、SO42- | B. | Na+、Mg2+、CO32-、Cl- | ||
| C. | K+、Ba2+、Cl-、Br- | D. | K+、Na+、SO42-、HCO3- |
| A. | Al与Fe2O3 | |
| B. | 电解熔融Al2O3 | |
| C. | 除去Al2O3的铝条浸在Hg(NO3)2溶液中 | |
| D. | A1与稀HCl |
| A. | 俄国化学家门捷列夫是通过实验的方法建立元素周期表的 | |
| B. | 现在我们课本上所列的元素周期表是由门捷列夫在1869年制定的 | |
| C. | 通常在元素周期表的右上方寻找制取催化剂的元素 | |
| D. | 元素的性质随着原子序数的递增而呈周期性变化 |
| A. | 该分子可能是天然蛋白质水解的产物 | |
| B. | 该分子核磁共振氢谱图可能有两个吸收峰,且面积之比为1:6 | |
| C. | 该分子只有2种同分异构体 | |
| D. | 分子中可能含有个一个羟基 |
| A. | 加热蒸干NaCl、MgCl2溶液时可以得到晶体NaCl、MgCl2 | |
| B. | 相同条件下,等物质的量浓度的溶液导电能力:HCl>NH3•H2O | |
| C. | 溶液中离子结合质子(氢离子)的能力:C2O42->HC2O4->SO42- | |
| D. | 海洋封存CO2会导致局部海洋水体酸性增强,会破坏海洋生态环境 |
| A. | a=b+m+n | B. | a=b-m+n | C. | a=b+m-n | D. | a=b-m-n |
| A. | 2H2+O2→2H2O+571.6 kJ | B. | 2H2(g)+O2(g)→2H2O(1)+142.9 kJ | ||
| C. | 2H2O(g)+O2(g)→2H2O(g)+571.6 kJ | D. | H2(g)+$\frac{1}{2}$O2(g)→H2O(1)+285.8 kJ |