题目内容
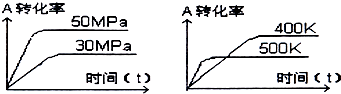 如图表示可逆反应mA(g)+nB(s)?xC(g)在不同温度和压强下,反应物A的转化率变化情况.下列判断正确的是( )
如图表示可逆反应mA(g)+nB(s)?xC(g)在不同温度和压强下,反应物A的转化率变化情况.下列判断正确的是( )| A、m>x,正反应为放热反应 |
| B、m+n<x,正反应为吸热反应 |
| C、m<x,正反应为放热反应 |
| D、m>x,正反应为吸热反应 |
考点:转化率随温度、压强的变化曲线
专题:
分析:增大压强,A的转化率增大,说明该反应的正反应是气体体积减小的反应,升高温度,A的转化率减小,说明正反应是放热反应,据此分析解答.
解答:
解:增大压强,A的转化率增大,说明该反应的正反应是气体体积减小的反应,则m>x;升高温度,A的转化率减小,说明正反应是放热反应,则△H<0,故选A.
点评:本题考查转化率图象分析,明确图象中纵横坐标的含义是解本题关键,根据温度、压强的改变对转化率、平衡移动的影响分析解答,题目难度不大.

练习册系列答案
相关题目
以下是一些常用的危险品标志,装运酒精的包装箱应贴的图标是( )
A、 |
B、 |
C、 |
D、 |
有一无色溶液,可能含有K+、A13+、Mg2+、NH4+、Cl-、SO42-、HCO3-、MnO4-中的几种.为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入盐酸酸化的BaCl2溶液,有白色沉淀产生.下列推断正确的是( )
| A、肯定有A13+、Mg2+、Cl- |
| B、肯定有A13+、Mg2+、NH4+ |
| C、肯定有K+、HCO3-、MnO4- |
| D、肯定有A13+、Mg2+、SO42- |
下列叙述Ⅰ和Ⅱ均正确并有因果关系的是( )
| A、较强酸可制较弱酸,次氯酸无法制盐酸 |
| B、Ca(OH)2能制成澄清石灰水,次氯酸无法制盐酸 |
| C、KNO3的溶解度大,用重结晶法除去KNO3中混有的NaCl |
| D、BaSO4难溶于酸,用盐酸和BaCl2溶液检验SO42- |
将20mL 0.5mol?L-1K2SO3溶液逐滴加入到20mL 0.2mol?L-1 硫酸酸化的紫色KMnO4溶液中,溶液恰好变为无色.则Mn元素在产物中的存在形态是( )
| A、Mn |
| B、Mn2+ |
| C、Mn2O3 |
| D、K2MnO4 |
某同学探究氨和铵盐的性质,相关实验操作及现象描述正确的是( )
| A、加热NH4Cl晶体制备氨气 |
| B、将蘸有浓氨水和浓硝酸的玻璃棒靠近,观察到白烟 |
| C、将氨水缓慢滴入AlCl3溶液中,研究Al(OH)3的两性 |
| D、室温下测定等浓度氨水和NaOH溶液的pH,比较N和Na的金属性强弱 |
下列关于化学反应速率的说法正确的是( )
| A、化学反应速率可用一定时间内任何一种反应物浓度的减小或生成物浓度的增加来表示 |
| B、化学反应速率0.8mol?L-1?s-1是指1s时某物质的浓度为0.8mol?L-1 |
| C、根据化学反应速率可以知道化学反应进行的快慢 |
| D、对于任何化学反应来说,反应速率越大,反应现象就越明显 |
下列变化中,属于吸热反应的是( )
| A、木炭燃烧反应 |
| B、酸碱中和反应 |
| C、铝和盐酸反应 |
| D、氢氧化钡晶体和氯化铵晶体反应 |