题目内容
某同学探究氨和铵盐的性质,相关实验操作及现象描述正确的是( )
| A、加热NH4Cl晶体制备氨气 |
| B、将蘸有浓氨水和浓硝酸的玻璃棒靠近,观察到白烟 |
| C、将氨水缓慢滴入AlCl3溶液中,研究Al(OH)3的两性 |
| D、室温下测定等浓度氨水和NaOH溶液的pH,比较N和Na的金属性强弱 |
考点:氨的化学性质,铵盐
专题:
分析:A.加热NH4Cl晶体,NH4Cl晶体易分解生成HCl和NH3,但HCl和NH3遇冷立即生成NH4Cl;
B.浓硝酸、浓氨水都具有挥发性,二者反应生成硝酸铵固体;
C.氨水不能溶解Al(OH)3;
D.N元素最高价氧化物的水化物呈酸性,一水合氨不是N元素的最高价氧化物的水化物,所以不能据此判断二者金属性强弱.
B.浓硝酸、浓氨水都具有挥发性,二者反应生成硝酸铵固体;
C.氨水不能溶解Al(OH)3;
D.N元素最高价氧化物的水化物呈酸性,一水合氨不是N元素的最高价氧化物的水化物,所以不能据此判断二者金属性强弱.
解答:
解:A.加热NH4Cl晶体,NH4Cl晶体易分解生成HCl和NH3,但HCl和NH3遇冷立即生成NH4Cl,所以不能用加热NH4Cl晶体制取氨气,应该用氯化铵和氢氧化钙制取氨气,故A错误;
B.浓硝酸、浓氨水都具有挥发性,二者相遇立即反应生成硝酸铵固体,有白烟生成,故B正确;
C.Al(OH)3能溶于强碱但不溶于弱碱,氨水不能溶解Al(OH)3,则不能利用氨水研究Al(OH)3的两性,故C错误;
D.N元素最高价氧化物的水化物是硝酸,呈酸性,一水合氨不是N元素的最高价氧化物的水化物,所以不能据此判断二者金属性强弱,故D错误;
故选B.
B.浓硝酸、浓氨水都具有挥发性,二者相遇立即反应生成硝酸铵固体,有白烟生成,故B正确;
C.Al(OH)3能溶于强碱但不溶于弱碱,氨水不能溶解Al(OH)3,则不能利用氨水研究Al(OH)3的两性,故C错误;
D.N元素最高价氧化物的水化物是硝酸,呈酸性,一水合氨不是N元素的最高价氧化物的水化物,所以不能据此判断二者金属性强弱,故D错误;
故选B.
点评:本题考查铵盐、氨气的性质,明确物质的性质是解本题关键,知道氨气的实验室制法、氢氧化铝的两性、非金属性和金属性强弱判断方法,注意氢氧化铝不溶于弱碱,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
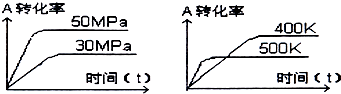 如图表示可逆反应mA(g)+nB(s)?xC(g)在不同温度和压强下,反应物A的转化率变化情况.下列判断正确的是( )
如图表示可逆反应mA(g)+nB(s)?xC(g)在不同温度和压强下,反应物A的转化率变化情况.下列判断正确的是( )| A、m>x,正反应为放热反应 |
| B、m+n<x,正反应为吸热反应 |
| C、m<x,正反应为放热反应 |
| D、m>x,正反应为吸热反应 |
下列情况下,埋在地下的输油铸铁管道被腐蚀最慢的是( )
| A、潮湿疏松透气的土壤中 |
| B、含铁元素较多的酸性土壤中 |
| C、干燥致密不透气的土壤中 |
| D、含碳量较高,潮湿透气的中性土壤中 |
下列溶液中含3种分子的是( )
| A、氯水 | B、溴的四氯化碳溶液 |
| C、醋酸溶液 | D、酒精水溶液 |
下列反应不属于氧化反应的是( )
| A、原电池的正极反应 |
| B、电解池的阳极反应 |
| C、金属的腐蚀 |
| D、煤的燃烧 |