题目内容
有一无色溶液,可能含有K+、A13+、Mg2+、NH4+、Cl-、SO42-、HCO3-、MnO4-中的几种.为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入盐酸酸化的BaCl2溶液,有白色沉淀产生.下列推断正确的是( )
| A、肯定有A13+、Mg2+、Cl- |
| B、肯定有A13+、Mg2+、NH4+ |
| C、肯定有K+、HCO3-、MnO4- |
| D、肯定有A13+、Mg2+、SO42- |
考点:常见离子的检验方法
专题:
分析:无色溶液中不含有色离子,则没有MnO4-;
①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解,则沉淀的成分是氢氧化镁和氢氧化铝;
②取部分溶液,加入盐酸酸化的BaCl2溶液,有白色沉淀产生,不溶于HCl的白色沉淀是硫酸钡沉淀,据此来回答问题.
①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解,则沉淀的成分是氢氧化镁和氢氧化铝;
②取部分溶液,加入盐酸酸化的BaCl2溶液,有白色沉淀产生,不溶于HCl的白色沉淀是硫酸钡沉淀,据此来回答问题.
解答:
解:无色溶液中不含有色离子,则没有MnO4-;
①取部分溶液,加入适量Na2O2固体,过氧化钠先是和水反应生成氢氧化钠和氧气,产生无色无味的气体是氧气,一定不是氨气,此时白色沉淀出现,再加入足量的NaOH溶液后白色沉淀部分溶解,则沉淀的成分是氢氧化镁和氢氧化铝,则证明其中一定含有A13+和Mg2+,一定不含有铵根离子、碳酸氢根离子(和铝离子不共存);
②取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生,和硫酸根离子反应生成白色不溶于硝酸的白色沉淀是硫酸钡沉淀,证明一定含有硫酸根离子;
综上可知肯定有A13+、Mg2+、SO42-.
故选D.
①取部分溶液,加入适量Na2O2固体,过氧化钠先是和水反应生成氢氧化钠和氧气,产生无色无味的气体是氧气,一定不是氨气,此时白色沉淀出现,再加入足量的NaOH溶液后白色沉淀部分溶解,则沉淀的成分是氢氧化镁和氢氧化铝,则证明其中一定含有A13+和Mg2+,一定不含有铵根离子、碳酸氢根离子(和铝离子不共存);
②取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生,和硫酸根离子反应生成白色不溶于硝酸的白色沉淀是硫酸钡沉淀,证明一定含有硫酸根离子;
综上可知肯定有A13+、Mg2+、SO42-.
故选D.
点评:本题考查了常见离子的检验,题目难度中等,注意明确常见离子的性质及检验的方法,特别是熟悉具有特殊现象的离子.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
大量事实证明,水溶液中并不存在H+、AlO2-等离子,实际存在的是H30+、[Al(OH)4]-.铝和强碱溶液的反应可以理解为铝在碱性环境下先与水反应,而后进一步与强碱反应(反应均不可逆).对于Al与重氢氧化钠(NaOD)的水溶液反应(假定水中不含氘和氚),下列说法正确的是( )
| A、生成的氢气中只含有D2 |
| B、生成的氢气中只含有H2 |
| C、生成的氢气中含有H2、HD、D2 |
| D、以上判断都不正确 |
如图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是( )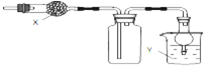

| A、X是碱石灰,收集到的气体是氯化氢,Y是水 |
| B、X是碱石灰,收集到的气体是氨气,Y是水 |
| C、X是氯化钙,搜集到的气体是二氧化硫,Y是氢氧化钠 |
| D、X是氯化钙,收集到的气体是一氧化氮,Y是氢氧化钠 |
关于Na2O和 Na2O2的叙述中错误的是( )
| A、Na2O是白色固体,Na2O2是淡黄色固体 |
| B、两物质都是碱性氧化物,其中氧元素的化合价都是-2价 |
| C、两者都能和水、二氧化碳、盐酸发生反应 |
| D、Na2O2比Na2O稳定,Na2O在一定条件下可转化为Na2O2 |
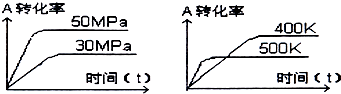 如图表示可逆反应mA(g)+nB(s)?xC(g)在不同温度和压强下,反应物A的转化率变化情况.下列判断正确的是( )
如图表示可逆反应mA(g)+nB(s)?xC(g)在不同温度和压强下,反应物A的转化率变化情况.下列判断正确的是( )| A、m>x,正反应为放热反应 |
| B、m+n<x,正反应为吸热反应 |
| C、m<x,正反应为放热反应 |
| D、m>x,正反应为吸热反应 |
下列溶液中含3种分子的是( )
| A、氯水 | B、溴的四氯化碳溶液 |
| C、醋酸溶液 | D、酒精水溶液 |
用足量的碳粉还原1mol金属氧化物,经充分反应生成的CO和CO2在标准状况下共40.32L,该金属氧化物可能是( )
| A、CuO |
| B、Fe3O4 |
| C、Al2O3 |
| D、PbO2 |