题目内容
A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去).

(1)若A是一种黄色单质固体,则B→C的化学方程式为 .
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为 ,试用化学方程式表示该物质与二氧化碳气体的反应 .将C长期露置于空气中,最后将变成物质D,D的化学式为 .现有D和NaHCO3的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38g,D的质量分数为 .

(1)若A是一种黄色单质固体,则B→C的化学方程式为
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为
考点:无机物的推断
专题:
分析:(1)A是一种黄色单质固体,应为S,则B为SO2,C为SO3;
(2)A是一种活泼金属,C是淡黄色固体,则A为Na,B为Na2O,C为Na2O2.
(2)A是一种活泼金属,C是淡黄色固体,则A为Na,B为Na2O,C为Na2O2.
解答:
解:(1)A是一种黄色单质固体,应为S,则B为SO2,C为SO3,SO2在催化剂条件下生成SO3,反应的方程式为2SO2+O2
2SO3,故答案为:2SO2+O2
2SO3;
(2)A是一种活泼金属,C是淡黄色固体,则A为Na,B为Na2O,C为Na2O2,过氧化钠与二氧化碳反应方程式为2Na2O2+2CO2═2Na2CO3+O2,
将过氧化钠长期露置于空气中,过氧化钠和水反应生成NaOH,NaOH和二氧化碳反应生成碳酸钠,过氧化钠和二氧化碳反应生成碳酸钠,所以最后将变成物质D,D的化学式为Na2CO3,加热时,固体减少的质量是二氧化碳和水,设碳酸钠的质量是x,则碳酸氢钠的质量是(10-x)g,
2NaHCO3
Na2CO3+CO2↑+H2O 固体减少质量
168g 62g
(10-x)g (10-9.38)g
168g:62g=(10-x)g:(10-9.38)g
解得x=8.32g,
则碳酸钠的质量分数=
×100%=83.2%,
故答案为:过氧化钠;2Na2O2+2CO2═2Na2CO3+O2;Na2CO3;83.2%.
| 催化剂 |
| △ |
| 催化剂 |
| △ |
(2)A是一种活泼金属,C是淡黄色固体,则A为Na,B为Na2O,C为Na2O2,过氧化钠与二氧化碳反应方程式为2Na2O2+2CO2═2Na2CO3+O2,
将过氧化钠长期露置于空气中,过氧化钠和水反应生成NaOH,NaOH和二氧化碳反应生成碳酸钠,过氧化钠和二氧化碳反应生成碳酸钠,所以最后将变成物质D,D的化学式为Na2CO3,加热时,固体减少的质量是二氧化碳和水,设碳酸钠的质量是x,则碳酸氢钠的质量是(10-x)g,
2NaHCO3
| ||
168g 62g
(10-x)g (10-9.38)g
168g:62g=(10-x)g:(10-9.38)g
解得x=8.32g,
则碳酸钠的质量分数=
| 8.32g |
| 10g |
故答案为:过氧化钠;2Na2O2+2CO2═2Na2CO3+O2;Na2CO3;83.2%.
点评:本题考查无机物的推断,题目难度不大,本题注意根据物质的颜色判断物质的可能性,易错点为氧化还原反应,注意电子的转移方向.

练习册系列答案
相关题目
某混合溶液中所含离子的浓度如下表,则M离子可能为( )
| 所含离子 | NO3- | SO42- | H+ | M |
| 浓度/(mol?L-1) | 2 | 1 | 2 | 1 |
| A、Na+ |
| B、Ba2+ |
| C、F- |
| D、S2- |
下列各组物质类别,在物质分类里前者从属于后者的一组是( )
| A、纯净物、混合物 |
| B、氧化物、化合物 |
| C、单质、化合物 |
| D、化合物、混合物 |
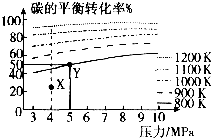 已知给煤炭加氢可发生反应:C(s)+2H2(g)?CH4(g).在VL的容器中投入amol碳(足量),同时通入2amolH2,控制条件使其发生上述反应,测得碳的平衡转化率随压强及温度的变化关系如下图所示.下列说法正确的是( )
已知给煤炭加氢可发生反应:C(s)+2H2(g)?CH4(g).在VL的容器中投入amol碳(足量),同时通入2amolH2,控制条件使其发生上述反应,测得碳的平衡转化率随压强及温度的变化关系如下图所示.下列说法正确的是( )| A、上述正反应为放热反应 | ||
| B、在4MPa、1200K时,图中X点v(H2)正>v(H2)逆 | ||
C、在5MPa、800K时,该反应的平衡常数为
| ||
| D、工业上维持6MPa1000K而不采用10MPa1000K,主要是因为前者碳的转化率高 |
下列有关说法正确的是( )
| A、钢铁的腐蚀过程中,析氢腐蚀与吸氧腐蚀不可能同时发生 |
| B、反应NH4Cl(s)=NH3(g)+HCl(g)在室温下不能自发进行,则该反应的△H>0 |
| C、由于Ksp(BaSO4)<Ksp(BaCO3),因此BaSO4沉淀不可能转化为BaCO3沉淀 |
| D、25℃时,0.1 mol?L-1CH3COOH溶液加水稀释后,c(OH-)/c(CH3COOH)增大 |