题目内容
卤化物和卤酸盐在工业生产中有着重要的作用.某小组为探究其中一些盐的性质,查阅资料并进行实验.查阅资料如下:
①BrO3-+6I-+6H+═3I2+Br-+3H2O
②2BrO3-+I2═2IO3-+Br2
③IO3-+5I-+6H+═3I2+3H2O
④2IO3-+10Br-+12H+═I2+5Br2+6H2O
实验如下:
请回答:
(1)根据资料中的反应①~④并结合所学知识,判断IO3-、BrO3-、I2、Br2的氧化性由强到弱的顺序是 ;KBrO3溶液与KBr溶液在酸性条件下反应的离子方程式是 .
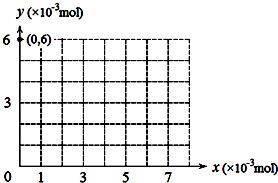
(2)若用y表示锥形瓶中含碘物质的物质的量,用x表示所滴入KBrO3的物质的量,在如图中画出上述整个实验过程中y随x的变化曲线(要求:在图中标出终点坐标).
①BrO3-+6I-+6H+═3I2+Br-+3H2O
②2BrO3-+I2═2IO3-+Br2
③IO3-+5I-+6H+═3I2+3H2O
④2IO3-+10Br-+12H+═I2+5Br2+6H2O
实验如下:
| 步骤 | 现象 |
| ⅰ.向盛有30mL 0.2mol?L-1 KI溶液的锥形瓶中依次滴入几滴淀粉溶液和足量稀硫酸,再用滴定管逐滴加入KBrO3溶液 | 随着KBrO3溶液滴入,溶液由无色变为蓝色并逐渐加深,最终保持不变 |
| ⅱ.继续向上述溶液中滴入KBrO3溶液 | 溶液的蓝色逐渐褪去 |
(1)根据资料中的反应①~④并结合所学知识,判断IO3-、BrO3-、I2、Br2的氧化性由强到弱的顺序是
(2)若用y表示锥形瓶中含碘物质的物质的量,用x表示所滴入KBrO3的物质的量,在如图中画出上述整个实验过程中y随x的变化曲线(要求:在图中标出终点坐标).

考点:氯、溴、碘及其化合物的综合应用,氧化还原反应
专题:元素及其化合物
分析:(1)根据氧化剂氧化性强于氧化产物的氧化性进行判断;KBrO3溶液与KBr溶液在酸性条件下,发生类似信息反应③的反应,BrO3-、Br-在酸性条件下生成溴单质与水;
(2)先发生①BrO3-+6I-+6H+=3I2+Br-+3H2O,0.006molI-完全反应生成0.003molI2、0.001molBr-,消耗0.001molBrO3-,再发生反应BrO3-+5Br-+6H+=3Br2+3H2O,0.001molBr-完全反应消耗0.0002molBrO3-,最后发生反应②2BrO3-+I2=2IO3-+Br2,0.003molI2完全反应生成0.006molIO3-,消耗0.006molBrO3-,据此作图.
(2)先发生①BrO3-+6I-+6H+=3I2+Br-+3H2O,0.006molI-完全反应生成0.003molI2、0.001molBr-,消耗0.001molBrO3-,再发生反应BrO3-+5Br-+6H+=3Br2+3H2O,0.001molBr-完全反应消耗0.0002molBrO3-,最后发生反应②2BrO3-+I2=2IO3-+Br2,0.003molI2完全反应生成0.006molIO3-,消耗0.006molBrO3-,据此作图.
解答:
解:(1)由反应①可知,氧化性BrO3->I2,由反应②可知,氧化性BrO3->IO3-,由反应③可知,氧化性IO3->I2,由反应④可知,氧化性IO3->Br2,故氧化性BrO3->IO3->Br2>I2;
BrO3-、Br-在酸性条件下生成溴单质与水,反应离子方程式为:BrO3-+5Br-+6H+=3Br2+3H2O,
故答案为:BrO3->IO3->Br2>I2;BrO3-+5Br-+6H+=3Br2+3H2O;
(2)先发生①BrO3-+6I-+6H+=3I2+Br-+3H2O,0.006molI-完全反应生成0.003molI2、0.001molBr-,消耗0.001molBrO3-,
再发生反应BrO3-+5Br-+6H+=3Br2+3H2O,0.001molBr-完全反应消耗0.0002molBrO3-,
最后发生反应②2BrO3-+I2=2IO3-+Br2,0.003molI2完全反应生成0.006molIO3-,消耗0.006molBrO3-,
故整个过程中含碘物质的物质的量,随加入KBrO3的物质的量的关系图为:
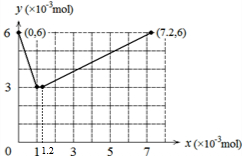
故答案为: .
.
BrO3-、Br-在酸性条件下生成溴单质与水,反应离子方程式为:BrO3-+5Br-+6H+=3Br2+3H2O,
故答案为:BrO3->IO3->Br2>I2;BrO3-+5Br-+6H+=3Br2+3H2O;
(2)先发生①BrO3-+6I-+6H+=3I2+Br-+3H2O,0.006molI-完全反应生成0.003molI2、0.001molBr-,消耗0.001molBrO3-,
再发生反应BrO3-+5Br-+6H+=3Br2+3H2O,0.001molBr-完全反应消耗0.0002molBrO3-,
最后发生反应②2BrO3-+I2=2IO3-+Br2,0.003molI2完全反应生成0.006molIO3-,消耗0.006molBrO3-,
故整个过程中含碘物质的物质的量,随加入KBrO3的物质的量的关系图为:

故答案为:
 .
.
点评:本题考查氧化还原反应及计算、对信息的利用,难度中等,是对学生综合能力的考查,(4)为易错点、难点,学生溶液忽略滴加过程中BrO3-氧化Br-的反应.

练习册系列答案
相关题目
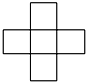 A、B、C、D、E五种主族元素所处周期表的位置如图所示,且原子序数依次由小到大.已知A元素能与氧元素形成化合物AO2,AO2中氧的质量分数为50%,且A原子中质子数等于中子数,则C元素在周期表的位置( )
A、B、C、D、E五种主族元素所处周期表的位置如图所示,且原子序数依次由小到大.已知A元素能与氧元素形成化合物AO2,AO2中氧的质量分数为50%,且A原子中质子数等于中子数,则C元素在周期表的位置( )| A、第三周期ⅥA族 |
| B、第三周期VA族 |
| C、第四周期ⅥA族 |
| D、第四周期VA族 |
近年来我国大部分地区出现雾霾天气,造成雾霾天气主要因素是( )
| A、SO2 |
| B、NO2 |
| C、PM2.5 |
| D、CO2 |
印刷铜质电路板的“腐蚀液”为FeCl3.已知铜、铁均能与FeCl3溶液反应,反应方程式分别为:Cu+2FeCl3═CuCl2+2FeCl2,FeCl3+2Fe═3FeCl2.现将一包铜铁的混合粉末放入到盛有FeCl3溶液的烧杯中,充分反应后烧杯仍有少量固体.关于烧杯中物质组成的说法正确的是( )
| A、溶液中一定含有FeCl2,固体中一定含有铜 |
| B、溶液中一定含有FeCl2、FeCl3,固体中一定含有铜和铁 |
| C、溶液中一定含有FeCl2、CuCl2,固体中一定含有铜 |
| D、溶液中一定含有FeCl2,固体只有铜 |
油脂的下列性质和用途中,与其含有不饱和碳碳双键有关的是( )
| A、油脂是产生能量最高的营养物质 |
| B、植物油通过氢化可以变为脂肪 |
| C、脂肪是有机体组织里储存能量的重要物质 |
| D、利用油脂在碱性条件下的水解,可以制甘油和肥皂 |
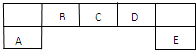 短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示:请回答下列问题:
短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示:请回答下列问题: “立方烷”是一种新合成的烃,其分子为正方体结构,其碳架结构如图所示.
“立方烷”是一种新合成的烃,其分子为正方体结构,其碳架结构如图所示.