题目内容
17.有关下列说法的判断正确的是( )| A. | 漂白粉在空气中不稳定,可用于漂白纸张 | |
| B. | 漂白粉中的CaCl2与空气中的CO2反应可生成CaCO3,漂白粉在空气中久置变质 | |
| C. | NH3能使酚酞溶液变红,因而NH3可用于设计喷泉实验 | |
| D. | 打磨磁石制指南针不涉及化学反应 |
分析 A.漂白粉在空气中与水、二氧化碳反应生成不稳定的次氯酸,用于漂白纸张为漂白性;
B.漂白粉中有效成分次氯酸钙和空气中二氧化碳水反应生成次氯酸和碳酸钙;
C.氨水溶液呈碱性,可使酚酞变红,为化学性质,形成喷泉,为物理性质;
D.打磨磁石制指南针,只是改变物质的外形,没有新物质生成.
解答 解:A.漂白粉在空气中与水、二氧化碳反应生成不稳定的次氯酸,用于漂白纸张为漂白性,表现性质不同,故A错误;
B.漂白粉中有效成分次氯酸钙和空气中二氧化碳水反应生成次氯酸和碳酸钙,次氯酸见光分解,漂白粉失效,故B错误;
C.氨气可用于设计喷泉实验是因为氨气极易溶于水,并非氨气能使酚酞变红,故C错误;
D.打磨磁石制指南针,只是改变物质的外形,没有新物质生成,不涉及化学反应,故D正确.
故选D.
点评 本题考查物质性质、物质的检验和鉴别,为高频考点,把握物质的性质及现象分析判断为解答的关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.在固定容积的容器中,某化学反应2A(g)?B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度( mol/L )随反应时间( min )的变化情况见表.
根据上述数据,完成下列填空:
(1)在实验1中,反应在10min至20min时间内平均速率v(A)为0.013mol/(L•min);达到平衡时A的转化率是50%,B的浓度是0.25mol/L;800℃时,该反应2A(g)?B(g)+D(g) 的平衡常数数值是0.25;若同温下,另一个恒容密闭的容器中也在发生该反应,某时刻A、B、D的浓度均为2mol/L,则该时刻v(正)<v(逆)(填“>”“=”或“<”).
(2)在实验2中,A的初始浓度c1=1.0mol/L,反应经20min就达到平衡,可推测实验2中还隐含的条件是使用了催化剂.
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3<v1(填“>”“=”或“<”),且c2> 1.0mol/L (填“>”“=”或“<”).
(4)比较实验4和实验1,可推测该反应是放热反应(填“吸热”或“放热”).
| 实验序号 | 温度 | 0min | 10min | 20min | 30min | 40min | 50min | 60min |
| 1 | 820℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 820℃ | c1 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c2 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 800℃ | 1.0 | 0.20 | 0.20 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)在实验1中,反应在10min至20min时间内平均速率v(A)为0.013mol/(L•min);达到平衡时A的转化率是50%,B的浓度是0.25mol/L;800℃时,该反应2A(g)?B(g)+D(g) 的平衡常数数值是0.25;若同温下,另一个恒容密闭的容器中也在发生该反应,某时刻A、B、D的浓度均为2mol/L,则该时刻v(正)<v(逆)(填“>”“=”或“<”).
(2)在实验2中,A的初始浓度c1=1.0mol/L,反应经20min就达到平衡,可推测实验2中还隐含的条件是使用了催化剂.
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3<v1(填“>”“=”或“<”),且c2> 1.0mol/L (填“>”“=”或“<”).
(4)比较实验4和实验1,可推测该反应是放热反应(填“吸热”或“放热”).
12.一定温度下的难溶电解质AmBn在水溶液中达到溶解平衡时,已知数据如表所示:
对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的溶液的说法,比较合理的( )
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| Ksp/25℃ | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
| A. | 向该混合溶液中加入少量铁粉即能观察到红色固体析出 | |
| B. | 向该混合溶液中逐滴加入NaOH溶液,最先看到蓝色沉淀 | |
| C. | 该混合溶液中c(SO42-):{c(Cu2+)+c(Fe2+)+c(Fe3+)}>5:4 | |
| D. | 向该混合溶液中加入适量氯水,并调节pH为3~4,然后过滤,可得到纯净的CuSO4溶液 |
2.要从含Al3+、Fe3+、Ba2+、Ag+的溶液中分别一一沉淀出Fe3+、Ba2+、Ag+,加入试剂的顺序正确的是( )
| A. | HCl、H2SO4、NH3•H2O | B. | NaOH、HCl、H2SO4 | ||
| C. | HCl、H2SO4、NaOH | D. | HCl、NaOH、H2SO4 |
7.下列各组混合物可用分液漏斗分离的一组是( )
| A. | 汽油和水 | B. | 碘和四氯化碳 | C. | 淀粉溶液和泥沙 | D. | 水和酒精 |



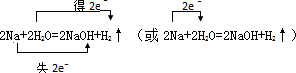 .反应中若产生0.2mol的气体,则有0.4mol的电子转移.
.反应中若产生0.2mol的气体,则有0.4mol的电子转移.