题目内容
8.在体积恒定的密闭容器中投入物质A和物质B在适宜的条件下发生反应:A(s)+2B(g)?2C(g)+D(g)(1)下列能表示该反应已达平衡状态的是 BD
A.2v(B)正=v(D)逆
B.混合气体的密度保持不变
C.混合气体中B、C、D的浓度之比为2:2:1
D.混合气体的压强不随时间变化而变化
(2)相同的压强下,充入一定量的A、B后,在不同温度下C的百分含量与时间的关系如图1所示.则T1>T2(填“>”、“<”或“=”),该反应的正反应的△H>0(填“>”、“<”或“=”).
(3)若该反应的逆反应速率与时间的关系如2图所示:

①由图可见,反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了条件,则t8时改变的条件是使用催化剂.
②若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系线.
(4)物质B在一定波长的光照射下发生分解反应,B的浓度随反应时间变化如图3所示,计算反应4~8min间的平均反应速率2.5mol•L-1•min-1,推测反应进行到16min时B的浓度约为2.5mol•L-1.
分析 (1)当化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度不再发生变化,由此衍生的一些物理性不变,据此解答;
(2)根据先拐先平衡,如图1T1>T2,温度高C的百分含量也大,所以升温平衡向正反应方向移动,故正反应为吸热反应;
(3)①t8后,正逆反应速率同等程度增大,反应前后气体体积不相同,只能是使用了催化剂;
②根据速率图象分析,根据t4时降压,平衡正向移动,t5时达到平衡,t6时增大反应物的浓度,平衡正向移动,分析绘制图象;
(4)根据v=$\frac{△c}{△t}$计算反应4~8min间的平均反应速率;0~4 min期间,反应物浓度变化为(40-20)mol/L=20mol/L,4~8 min期间,反应物浓度变化为(20-10)mol/L=10μmol/L,可知,每隔4分钟,速率降为原来的一半,据此计算.
解答 解:(1)A.V正(B)=2V逆(D),说明正逆反应速率相等,才可以判断是否达到平衡状态,故A错误;
B.A为固体,反应正向进行时气体质量增大,密度增大,所以密度不变时反应达到平衡状态,故B正确;
C.混合气体中B、C、D的浓度之比为2:2:1不能说明正逆反应速率相等,不能判断是否达到平衡状态,故C错误;
D.该反应是一个反应前后气体体积改变的反应,混合气体的总压强不变,该反应达到平衡状态,故D正确;
故选:BD;
(2)根据先拐先平衡,如图1T1>T2,温度高C的百分含量也大,所以升温平衡向正反应方向移动,故正反应为吸热反应,
故答案为:>;>;
(3)①t8后,正逆反应速率同等程度增大,反应前后气体体积不相同,只能是使用了催化剂,
故答案为:使用催化剂;
②t4时降压,则逆反应速率瞬间变小后逐渐增大,平衡正向移动,t5时达到平衡逆反应速率不变,t6时增大反应物的浓度,逆反应瞬间没变,但随后速率也会慢慢增加,所以请在图2中画出t4~t6时逆反应速率与时间的关系线如图: ,
,
故答案为: ;
;
(4)由图可知,4~8 min期间,反应物浓度变化为(20-10)mol/L=10mol/L,
所以4~8 min期间,反应速率为$\frac{10mol/L}{4min}$=2.5 mol/(L•min);
由图可知,0~4 min期间,反应物浓度变化为(40-20)mol/L=20mol/L,4~8 min期间,反应物浓度变化为(20-10)mol/L=10mol/L,可知,每隔4分钟,浓度变化量降为原来的一半,所以8~12min浓度变化为5 mol/L,12~16min浓度变化为2.5 mol/L,
所以16min时浓度为10 mol/L-5 mol/L-2.5 mol/L=2.5 mol/L,
故答案为:2.5 mol/(L•min);2.5 mol/L.
点评 本题考查了化学平衡状态的判断及有关计算,本题的亮点在于连续多个条件改变引起v-t图的变化,更有意思的是学生习惯于v正、v逆一起画,而本题只要求单画v逆,这打破了考生的思维定势,对于学生在真正考中顺利解答此类问题有着积极的作用.

| A. | 矿泉水 | B. | 蒸馏水 | C. | 自来水 | D. | 雨水 |
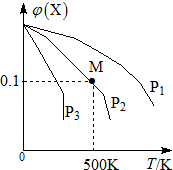 某可逆反应为2X(g)?3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示,下列推断正确的是( )
某可逆反应为2X(g)?3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示,下列推断正确的是( )| A. | 在该条件下M点X平衡转化率为$\frac{9}{11}$ | |
| B. | 压强大小有P3>P2>P1 | |
| C. | 平衡后加入高效催化剂使气体相对分子质量增大 | |
| D. | 升高温度,该反应平衡常数K减小 |
实验 序号 | 时间 浓度 温 度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | c1 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | 1.0 | c2 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)实验1达到平衡的时间是40min,实验4达到平衡的时间是30min.
(2)C1大于C2 (填“大于”“小于”“等于”);C3=1.0mol•L-1
(3)实验4比实验1的反应速率快(填“快”或“慢”),原因是实验4的温度比实验1高,温度越高,反应越快
(4)如果2A (g)?B(g)+D(g) 是一个放热反应,那么实验4与实验1相比,实验1 放出的热量多,理由是升高温度平衡向逆方向移动.
| A. | 漂白粉在空气中不稳定,可用于漂白纸张 | |
| B. | 漂白粉中的CaCl2与空气中的CO2反应可生成CaCO3,漂白粉在空气中久置变质 | |
| C. | NH3能使酚酞溶液变红,因而NH3可用于设计喷泉实验 | |
| D. | 打磨磁石制指南针不涉及化学反应 |
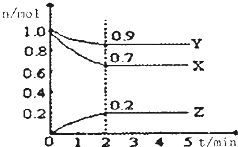 某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的两随时间的变化曲线如图所示,据此回答:
某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的两随时间的变化曲线如图所示,据此回答: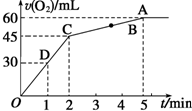 加入0.1mol MnO2粉末于50mL过氧化氢溶液(ρ=1.1g•mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示.
加入0.1mol MnO2粉末于50mL过氧化氢溶液(ρ=1.1g•mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示. .
.