题目内容
硫酸镁常用作制革、炸药、造纸、瓷器、肥料,以及医疗上口服泻药等.已知25℃时,Ksp[Mg(OH)2]=1.0×10-11,Kw=1.0×10-14,Ksp(CaSO4)=9.1×10-6,则下列说法正确的是( )
| A、水是一种极弱的电解质,存在电离平衡H2O?H++OH-.在水中加入少量MgSO4固体时,上述平衡将向正反应方向移动,KW增大 |
| B、在MgSO4溶液中各离子浓度关系:c(Mg2+)+c(OH-)=c(OH-)+c(SO42-) |
| C、向1L0.01 mol.L-1MgSO4溶液中加入1L 0.001 mol.L-1CaCl2溶液即可生成CaSO4沉淀 |
| D、若溶液中某离子的浓度低于1.0×10-5mol.L-1即可认为该离子被除尽,常温下要出去0.1 mol.L-1MgSO4溶液中的Mg2+,至少要调节pH≥11. |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:A、KW是只与温度有关的一个物理量;
B、根据溶液中电荷守恒,知2c(Mg2+)+c(H+)=c(OH-)+2c(SO42-);
C、根据Ksp(CaSO4)=9.1×10-6,若c(Ca2+)?c(SO42-)>9.1×10-6,则有沉淀生成,若小于等于Ksp(CaSO4),则没有沉淀生成;
D、要除去Mg2+,则使c(Mg2+)<1.0×10-5mol.L-1.
B、根据溶液中电荷守恒,知2c(Mg2+)+c(H+)=c(OH-)+2c(SO42-);
C、根据Ksp(CaSO4)=9.1×10-6,若c(Ca2+)?c(SO42-)>9.1×10-6,则有沉淀生成,若小于等于Ksp(CaSO4),则没有沉淀生成;
D、要除去Mg2+,则使c(Mg2+)<1.0×10-5mol.L-1.
解答:
解:A、KW是只与温度有关的一个物理量,和加入的物质无关,故A错误;
B、根据溶液显电中性,2c(Mg2+)+c(H+)=c(OH-)+2c(SO42-),故B错误;
C、根据Ksp(CaSO4)=9.1×10-6,若c(Ca2+)?c(SO42-)>9.1×10-6,则有沉淀生成,加入1L 0.001 mol.L-1CaCl2溶液后,c(Ca2+)?c(SO42-)=(
×0.01 mol.L-1)×(
×0.001 mol.L-1)=2.5×10-6<9.1×10-6,故C错误;
D、要除去Mg2+,则使c(Mg2+)<1.0×10-5mol.L-1,根据Ksp[Mg(OH)2]=c(Mg2+)?c2(OH-)=1.0×10-11,解得c(OH-)=1.0×10-3,pH=11,故D正确.
故选:D.
B、根据溶液显电中性,2c(Mg2+)+c(H+)=c(OH-)+2c(SO42-),故B错误;
C、根据Ksp(CaSO4)=9.1×10-6,若c(Ca2+)?c(SO42-)>9.1×10-6,则有沉淀生成,加入1L 0.001 mol.L-1CaCl2溶液后,c(Ca2+)?c(SO42-)=(
| 1 |
| 2 |
| 1 |
| 2 |
D、要除去Mg2+,则使c(Mg2+)<1.0×10-5mol.L-1,根据Ksp[Mg(OH)2]=c(Mg2+)?c2(OH-)=1.0×10-11,解得c(OH-)=1.0×10-3,pH=11,故D正确.
故选:D.
点评:本题考查溶度积的有关计算,难度中等,注意计算时容易忽略混合后溶液的浓度发生变化.

练习册系列答案
相关题目
下列有关实验操作、现象或实验原理叙述错误的是( )
| A、纸层折法分离Fe3+和Cu2+的实验中,点样后的滤纸需晾干后可使用 |
| B、在中和热测定的实验中,可将反应前氢氧化钠溶液的温度作为起始温度 |
| C、将Kcl和NaNO3的混合液加热并浓缩至有晶体析出时,趁热过滤可分离得NaCl晶体 |
| D、(镀锌铁皮锌镀层厚度的测定)实验中,当锌完全溶解后,铁与酸反应产生氢气的速率会显著减慢,借此可判断锌镀层是否反应完全 |
某溶液中含有SO42-、SO32-、SiO32-、CO32-、Na+,向该溶液中通入过量的Cl2,
下列判断正确的是( )
①反应前后,溶液中离子浓度基本保持不变的有SO42-、Na+;
②有白色胶状物质生成;
③有气体产生;
④发生了氧化还原反应.
下列判断正确的是( )
①反应前后,溶液中离子浓度基本保持不变的有SO42-、Na+;
②有白色胶状物质生成;
③有气体产生;
④发生了氧化还原反应.
| A、①②③④ | B、②③④ |
| C、①②③ | D、②③ |
下列溶液中有关微粒的物质的量浓度关系正确的是( )
| A、NaHSO3和NaHCO3的中性混合溶液中:c(Na+)=c(HSO3-)+2c(SO32-)+c(HCO3-)+2c(CO32-) |
| B、常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后溶液中:c(Na+)>c(Cl-)>c(CH3COOH) |
| C、常温下物质的量浓度相等的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2三种溶液中c(NH4+):①<②<③ |
| D、等体积物质的量浓度的NaClO(aq)与NaCl(aq)中离子总数多少:N前>N后 |
有①氨水、②NH4Cl溶液、③Na2CO3溶液、④NaHCO3溶液各25mL,物质的量浓度均为0.1mol/L,下列说法正确的是( )
| A、4种溶液pH的大小顺序:①>④>③>② |
| B、溶液①、②等体积混合后pH>7,则c(NH4+)<c(NH3?H2O) |
| C、向溶液①、②中分别加入25 mL 0.1mol/L 盐酸后,溶液中c(NH4+):①>② |
| D、向溶液③、④中分别加入25mL 0.1mol/L NaOH溶液后,两溶液中的离子种类相同 |
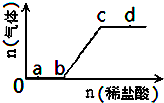 向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列粒子组在对应的溶液中一定能大量共存的是( )
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列粒子组在对应的溶液中一定能大量共存的是( )| A、a点对应的溶液中:Na+、SO42-、NO3-、Fe(OH)3胶体微粒 |
| B、b点对应的溶液中:Al3+、H+、MnO4-、Cl- |
| C、c点对应的溶液中:Na+、Ca2+、NO3-、Cl- |
| D、d点对应的溶液中:F-、NO3-、Fe2+、Ag+ |
下列说法不正确的是( )
| A、硅单质可用于光纤通讯 |
| B、由SiO2制取硅酸,可先使SiO2与NaOH溶液反应,再通入CO2 |
| C、青石棉[Na2Fe5Si8O22(OH)2]的化学组成可表示为:Na2O?3FeO?Fe2O3?8SiO2?H2O |
| D、Na2SiO3可用于制备木材防火剂 |
下列说法正确的是( )
| A、氢氧燃料电池的能量转换形式之一为化学能转化为电能 |
| B、铅蓄电池放电时的负极和充电时的阴极均发生氧化反应 |
| C、电解精炼铜过程中,阳极质量的减少与阴极质量的增加一定相等 |
| D、催化剂通过降低化学反应的焓变加快化学反应速率 |
