��Ŀ����
11��ԭ���������������X��Y��Z��M��WΪ���ֶ�����Ԫ�أ���֪Y��Z��M��W�ֱ�ͬ���ڣ�X��Mͬ���壻X��Z��M��Z�����Էֱ��γ�A2B��A2B2�͵Ļ����X��Y�γɵ���̬�������ڱ�״���µ��ܶ�Ϊ0.76g•L-1��Y��M��W������������ˮ��������䶼�ܷ�����Ӧ������˵������ȷ���ǣ�������| A�� | ��X��Y��Z����Ԫ���γɵ�ij�ֻ�������ܺ������Ӽ� | |
| B�� | ����Ԫ�طֱ��γɵĵ��������У�M�����Ӱ뾶��� | |
| C�� | W���Ȼ�������һ��10e-���Ӻ�һ��18e-���ӹ��ɵ� | |
| D�� | XԪ����Z��������ĸ�Ԫ���γɵ�A2B�ͻ�������X2Z�е���� |
���� ԭ���������������X��Y��Z��M��WΪ���ֶ�����Ԫ�أ�X��Y�γɵ���̬�������ڱ�״���µ��ܶ�Ϊ0.76g•L-1�������̬���������Է�������=0.76��22.4=17��ӦΪNH3������֪XΪHԪ�ء�YΪNԪ�أ�X��Mͬ���壬Mԭ����������NԪ�أ���MΪNa��Y��Zͬ���ڣ�X��Z��M��Z�����Էֱ��γ�A2B��A2B2�͵Ļ������ZΪOԪ�أ�M��W�ֱ�ͬ���ڣ�X��Z��M��������֮�͵���Y��W��������֮�ͣ���M��Wԭ���������1+8-7=2������֪WΪAlԪ�أ�Y��M��W������������ˮ��������䶼�ܷ�����Ӧ���������⣬�Դ˽����⣮
��� �⣺XΪHԪ�ء�YΪNԪ�أ�ZΪOԪ�أ�MΪNa��WΪAlԪ�أ�
A��XΪHԪ�ء�YΪNԪ�أ�ZΪOԪ�أ�������Ǻ������Ӽ������ӻ������A��ȷ��
B�����Ӳ�ṹ��ͬ�˵����Խ��뾶ԽС�������Ƶ����Ӱ뾶���B��ȷ��
C���Ȼ�������һ��10e-�����Ӻ�һ��18e-�����ӹ��ɣ���C��ȷ��
D��ˮ���Ӽ��������е���ߣ���������ͣ���D����
��ѡD��
���� ���⿼��Ԫ���ƶϡ�Ԫ�������ɡ����ӽṹ��C��N��NaԪ�ػ��������ʵȣ�Ϊ��Ƶ���㣬������ѧ���ķ��������Ŀ��飬�Ѷ��еȣ������ܶ��ж�X��Y�γɵ���̬�������ǰ������ƶϵĹؼ���

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�| A�� | Ϊ��ֹ�����⣬�������Ϳһ��������� | |
| B�� | Ϊ��ֹ���֣�����۳�������վ�ȳ���Ҫ�Ͻ��̻� | |
| C�� | Ϊ�ӿ�H2O2�ķֽ����ʣ��ѷ�Ӧ�����ŵ���ˮ����ȴ | |
| D�� | Ϊ�ӿ�KClO3�ķֽ����ʣ�����MnO2 |
 ���ȱ�������һ��ҩ���м��壬���ö��ȼױ�Ϊԭ�ϣ�ͨ����������������Ʊ�����Ӧ���£�
���ȱ�������һ��ҩ���м��壬���ö��ȼױ�Ϊԭ�ϣ�ͨ����������������Ʊ�����Ӧ���£���
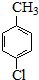 $��_{����}^{KMnO_{4}}$
$��_{����}^{KMnO_{4}}$
��
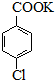 $\stackrel{H+}{��}$
$\stackrel{H+}{��}$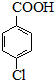
�йػ�����������������±���
| �۵�/�� | �е�/�� | �ܶ�/g•cm��3 | ��ɫ | ˮ���� | |
| ���ȼױ� | 7.5 | 162 | 1.07 | ��ɫ | ���� |
| ���ȱ����� | 243 | 275 | 1.54 | ��ɫ | �� |
| ���ȱ������ | �����ε�ͨ�ԣ����ڿ������Σ��ܽ�����¶����߶����� | ||||
���ڹ��Ϊ250mL��������ƿ��װ��A���м���һ�����Ĵ���������KMnO4��100mLˮ��
����ͼ��װ��װ�ã��ڷ�Һ©����װ��C���м���6.00mL���ȼױ���������93��ʱ����ε�����ȼױ���
�ۿ����¶���93�����ң���Ӧ2h���ˣ�ϴ����������ϴ��Һ����Һ�ϲ�������ϡ�����ữ��
�ܼ���Ũ������ȴ�ᾧ�����ˣ�ϴ����������������������Ϊwg��
��ش��������⣺
��1��װ��B�������������ܣ�
��2�������й�ʵ���˵������ȷ����AB
A����ȡ6.00mL���ȼױ���ѡ��25mL��ʽ�ζ���
B��װ��B��ˮ������ɴ�b�ڽ�a�ڳ�
C�������¶���93�����ң���ò���ˮԡ����
D��ȡ��������һ��ϴ��Һ�������Թ��У������е���BaCl2��Һ���ɼ��������Ƿ�ϴ�Ӹɾ�
��3��������ж��ȼױ��ļ��뷽������μ��������һ���Լ��룬�����Ǽ��ٶ��ȼױ��Ļӷ������ԭ�������ʣ�
��4��������й��˵�Ŀ���dz�ȥMnO2����Һ�м���ϡ�����ữ���ɹ۲쵽��ʵ�������Dz�����ɫ������
��5��ϴ����������ʵ�ϴ�Ӽ����������C���������B��
A���Ҵ� B����ˮ C����ˮ D����Һ
��6������M1��ʾ���ȼױ���ʽ����M2��ʾ���ȱ������ʽ������ʵ����ʵļ������ʽΪ$\frac{w}{\frac{6��1.07{M}_{2}}{{M}_{1}}}$��100%����Ҫ����㣩��
| A�� | ��ˮ��ȣ�AgCl��Na2CO3��Һ�е��ܽ�ȼ��ܶȻ������� | |
| B�� | ��Ӧ�����Һ�У�c��Na+����c��CO32-����c��Cl-��=c��Ag+����c��OH-����c��H+�� | |
| C�� | ��Һ��c��Cl-��=2��10-5mol•L-1 | |
| D�� | ����ת����Ӧ��2AgCl��s��+CO32-��aq��?Ag2CO3��s��+2Cl-��aq����ƽ�ⳣ��Ϊ2��10-9 |

ʵ�飨һ�����������ȡ
����1��ȡ14.40g�����ǣ���Է�������Ϊ180���ձ��У���������������������ͣ�72Сʱ���ˣ�����Һת�Ƶ�����A�У����ݣ��õ�500mLԭҺ��
����2��ȡ20.00mLԭҺ����ƿ�У������̪��ָʾ������ŨΪ0.1000mol/L��NaOH��Һ�ζ����յ㣬�ظ�4�Σ����ݼ�¼���±������ٶ�ԭҺ���������ʲ���NaOH��Ӧ��
| ���� | 1 | 2 | 3 | 4 |
| ������mL�� | 19.22 | 19.18 | 19.80 | 19.20 |
��2������ж��ѵ���ζ��յ㵱�������һ�α�Һʱ����ƿ����ɫ��Һ���ɫ���Ұ�����ڲ���ɫ��
��3������IJ���Ϊ30%��
ʵ�飨���������������
��֪�����Ka=1.4��10-4��̼���Ka1=4.47��10-3
��4�����ʵ��֤�����������ȡ0.1mol/L������Һ���ձ��У���PH�Ʋⶨ��PHֵ����PH����1��˵�����������������ȡ0.1mol/L��������Һ���ձ��У���pH�Ʋⶨ��PHֵ����PH����7��˵�����������ᣩ��ȡPH=a������Һ���ձ��У���ˮϡ��10n������PH�Ʋⶨ��PHֵ����PHС��a+n˵�����������ᣩ��
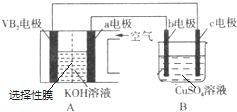
��5��С��������ͼ��ʾ��������ҩƷ��ͨ��ʵ�����Ƚ�������̼�������ǿ����

�ٿɹ۲쵽�ձ��е���������Һ���ְ�ɫ���ǣ�д���ձ��з����Ļ�ѧ��Ӧ����ʽ2NaAlO2+3H2O+CO2�T2Al��OH��3��+Na2CO3��NaAlO2+2H2O+CO2�TAl��OH��3��+NaHCO3��
��ѧϰС�����г�Ա�������ʵ����Ʋ����Ͻ�����������Ľ��Ĵ�ʩ��A��B֮������һ��װ��̼��������Һ��ϴ��ƿ��
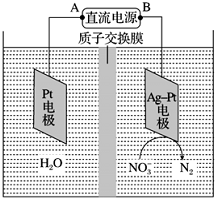 �绯ѧ����NO3-��ԭ����ͼ��ʾ��
�绯ѧ����NO3-��ԭ����ͼ��ʾ�� ����Ԫ�غ�����ߵ����ķ���ʽCH4��
����Ԫ�غ�����ߵ����ķ���ʽCH4��