题目内容
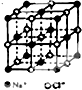 氯化钠是生活中的常用调味品,也是结构化学中研究离子晶体时常用的代表物,其晶胞结构如图所示.
氯化钠是生活中的常用调味品,也是结构化学中研究离子晶体时常用的代表物,其晶胞结构如图所示.(1)设氯化钠晶体中Na+与跟它最近邻的Cl-之间的距离为r,则该Na+与跟它次近邻的C1-个数为
(2)已知在氯化钠晶体中Na+的半径为以a pm,Cl-的半径为b pm,它们在晶体中是紧密接触的,则在氯化钠晶体中离子的空间利用率为
(3)纳米材料的表面原子占总原子数的比例很大,这是它有许多特殊性质的原因.假设某氯化钠颗粒形状为立方体,边长为氯化钠晶胞的10倍,则该氯化钠颗粒中表面原子占总原子数的百分比为
考点:晶胞的计算
专题:
分析:(1)根据NaCl晶体结构判断:Na+位于顶点与它次近邻的Cl-位于晶胞的体心位置,据此判断次近邻的Cl-数目和距离;
(2)NaCl晶胞为面心立方密堆积,则晶胞的边长为(2a+2b)pm,计算出Na+和Cl-所占体积和晶胞体积,从而计算出空间利用率;
(3)氯化钠颗粒边长为晶胞边长的10倍,则每条边含有的原子数为21个,则总原子数为21的立方,表面原子总数为总原子数减去内部总原子数,内部原子总数相当于剥掉了一层晶胞,即颗粒内部每条边有19个原子,则内部原子总是为19的立方,据此计算该氯化钠颗粒中表面原子占总原子数的百分比.
(2)NaCl晶胞为面心立方密堆积,则晶胞的边长为(2a+2b)pm,计算出Na+和Cl-所占体积和晶胞体积,从而计算出空间利用率;
(3)氯化钠颗粒边长为晶胞边长的10倍,则每条边含有的原子数为21个,则总原子数为21的立方,表面原子总数为总原子数减去内部总原子数,内部原子总数相当于剥掉了一层晶胞,即颗粒内部每条边有19个原子,则内部原子总是为19的立方,据此计算该氯化钠颗粒中表面原子占总原子数的百分比.
解答:
解:(1)Na+位于顶点,被8个晶胞共有,即Na+与跟它次近邻的Cl-个数为8;Na+与跟它次近邻的Cl-之间的距离为晶胞体对角线的一半,距离为
r,
故答案为:8;
r;
(2)晶胞中共含有4个Na+和4个Cl-,体积为:
π(a3+b3)×4,晶胞的边长为a+b,晶胞体积为(2a+2b)3,氯化钠晶体中离子的空间利用率为
=
×
×100%,故答案为
×
×100%;
(3)氯化钠颗粒边长为晶胞边长的10倍,则每条边含有的原子数为21个,则总原子数为21的立方,表面原子总数为总原子数减去内部总原子数,内部原子总数相当于剥掉了一层晶胞,即颗粒内部每条边有19个原子,则内部原子总是为19的立方,该氯化钠颗粒中表面原子占总原子数的百分比为
×100%=26%,
故答案为:26%.
| 3 |
故答案为:8;
| 3 |
(2)晶胞中共含有4个Na+和4个Cl-,体积为:
| 4 |
| 3 |
| ||
| (2a+2b)3 |
| 2π |
| 3 |
| (a3+b3) |
| (a+b)3 |
| 2π |
| 3 |
| (a3+b3) |
| (a+b)3 |
(3)氯化钠颗粒边长为晶胞边长的10倍,则每条边含有的原子数为21个,则总原子数为21的立方,表面原子总数为总原子数减去内部总原子数,内部原子总数相当于剥掉了一层晶胞,即颗粒内部每条边有19个原子,则内部原子总是为19的立方,该氯化钠颗粒中表面原子占总原子数的百分比为
| 213-193 |
| 213 |
故答案为:26%.
点评:点评:本题考查物质结构和性质,涉及晶胞的计算等知识点,难点是晶胞的计算和氯化钠颗粒中表面原子占总原子数的百分比的计算,灵活运用公式是解本题关键,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列实验方法或操作:
①用100mL筒量配制60mL10% 的盐酸;②称量没有腐蚀性固体药品时,把药品放在托盘上称量;③浓硫酸沾到皮肤上要先用抹布擦再用大量水冲洗;④用托盘天平称取5.20gNaCl晶体;⑤蒸馏开始时应先加热在开冷凝水;⑥萃取操作时选择的萃取剂的密度不必比水大;⑦用容量瓶配制一定浓度的某溶液后,将溶液保存在容量瓶中并贴上标签.其中正确的是( )
①用100mL筒量配制60mL10% 的盐酸;②称量没有腐蚀性固体药品时,把药品放在托盘上称量;③浓硫酸沾到皮肤上要先用抹布擦再用大量水冲洗;④用托盘天平称取5.20gNaCl晶体;⑤蒸馏开始时应先加热在开冷凝水;⑥萃取操作时选择的萃取剂的密度不必比水大;⑦用容量瓶配制一定浓度的某溶液后,将溶液保存在容量瓶中并贴上标签.其中正确的是( )
| A、③⑥ | B、②③⑦ |
| C、①③⑥ | D、③⑤⑥ |
工业上常用焦炭和二氧化硅在电炉中发生反应制取粗硅,化学方程式;SiO2+2C
Si+2CO.下列说法不正确的是( )
| ||
| A、该反应属于置换反应 |
| B、C是还原剂,发生还原反应 |
| C、SiO2是氧化剂,在反应中还原 |
| D、氧化还原反应的实质是电子的转移 |
为了使Na2S溶液中
的比值变小,可适量加入(或通入)的物质是( )
| c(Na+) |
| c(S2-) |
| A、H2S气体 |
| B、NaOH固体 |
| C、HCl气体 |
| D、KOH固体 |
下列关于钠的叙述中不正确的是( )
| A、钠具有很强的还原性 |
| B、钠原子的最外层只有一个电子 |
| C、在实验室中,钠通常保存在石蜡油或煤油中 |
| D、钠在常温下不易被氧化 |
在电解质溶液的导电性装置中,若向某一电解质溶液中逐滴加入另一种溶液,则灯泡由亮变暗,至熄灭后又逐渐变亮的是( )
| A、将浓盐酸逐滴加入食盐溶液 |
| B、将硫酸逐滴加入氢氧化钡溶液 |
| C、将硫酸逐滴加入氢氧化钠溶液 |
| D、将浓盐酸逐滴加入氢氧化钠溶液 |
已知化学反应2C(s)+O2(g)═2CO(g),2CO(g)+O2(g)=2CO2(g)都是放热反应.据此判断,下列说法中不正确的是( )
| A、1.2gC所具有的能量一定高于28gCO所具有的能量 |
| B、56g CO和32g O2所具有的总能量大于88g CO2所具有的总能量 |
| C、12g C和32g O2所具有的总能量大于44g CO2所具有的总能量 |
| D、将一定质量的C燃烧,生成CO2比生成CO时放出的热量多 |