题目内容
已知次氯酸分子的结构式为H-O-Cl,下列有关说法正确的是( )
| A、O原子发生sp杂化 |
| B、O原子与H、Cl都形成σ键 |
| C、该分子为直线型分子 |
| D、该分子Cl原子显-1价 |
考点:不同晶体的结构微粒及微粒间作用力的区别,判断简单分子或离子的构型,原子轨道杂化方式及杂化类型判断
专题:化学键与晶体结构
分析:A、通过价层电子对互斥理论计算中心原子的价层电子对数,判断杂化类型;
B、共价单键为σ键;
C、HClO中O的价层电子对数为4,孤电子对数为2,空间构型为V型
D、次氯酸中Cl为+1价,O为-2价,H为+1价.
B、共价单键为σ键;
C、HClO中O的价层电子对数为4,孤电子对数为2,空间构型为V型
D、次氯酸中Cl为+1价,O为-2价,H为+1价.
解答:
解:A、HClO中O原子形成2个σ键,孤电子对个数=
×(6-2×1)=2,价层电子对数为4,为sp3杂化,故A错误;
B、从次氯酸的结构式可以看出含有O-H、O-Cl,共价单键为σ键,故B正确;
C、HClO中O价层电子对数为4,孤电子对数为2,空间构型为V型,故C错误;
D、次氯酸中Cl为+1价,O为-2价,H为+1价,故D错误;
故选B.
| 1 |
| 2 |
B、从次氯酸的结构式可以看出含有O-H、O-Cl,共价单键为σ键,故B正确;
C、HClO中O价层电子对数为4,孤电子对数为2,空间构型为V型,故C错误;
D、次氯酸中Cl为+1价,O为-2价,H为+1价,故D错误;
故选B.
点评:本题考查了次氯酸分子的结构,明确中心原子杂化类型的判断是解答本题的关键,题目难度中等.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
若ag某气体中含有的分子数为b,则cg该气体的物质的量为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列有关晶体的大小比较不正确的是( )
| A、阴离子的配位数:CsCl>NaCl>CaF2 |
| B、热分解温度:BaCO3>CaCO3>MgCO3 |
| C、熔点:NaF>MgF2>AlF3 |
| D、硬度:C3N4>金刚石>碳化硅 |
根据物质的熔点、沸点数据,推断错误的是( )
| 晶体 | NaCl | MgO | AlCl3 | SiCl4 | B(硼) |
| 熔点℃ | 801 | 2852 | 180 | -70 | 2300 |
| 沸点℃ | 1465 | --- | 177 | 57 | 2500 |
| A、晶体的沸点CCl4<SiCl4 |
| B、在火山喷出的岩浆,晶出顺序为MgO先于NaCl |
| C、用AlCl3通过电解法冶炼铝 |
| D、硼的硬度大,不溶于水,但能与NaOH溶液反应 |
下列表示对应化学反应的离子方程式正确的是( )
A、向氯化铝溶液通入过量的氨气:Al3++4OH-═
| ||||
B、MnO2与浓盐酸反应制Cl2:MnO2+4HCl
| ||||
| C、FeCl3溶液用于蚀刻印刷电路:Cu+2Fe3+=Cu2++2Fe2+ | ||||
| D、在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+Fe(OH)3=FeO42-+3Cl-+H2O+4H+ |
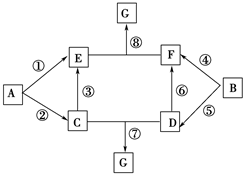 A~G的转化关系如图所示(部分反应物、产物和反应条件未标出).
A~G的转化关系如图所示(部分反应物、产物和反应条件未标出).