题目内容
写出下列各烷烃的分子式.
(1)某烷烃1.16克与氧气完全燃烧,生成二氧化碳3.52克,通过计算确定该烃的分子式. .
(2)标准状况下,体积为1.12L的含碳原子为n 和n+2个的两种气态烷烃的混合物质量为1.8克,试通过计算确定两种气态烷烃各是 .(填分子式)
(3)分子中含有31个共价键的烷烃D为 .(填分子式)
(4)室温下相对分子质量最大的气态烷烃F为 .(填分子式)
(5)写出甲苯的一氯取代有机产物的结构简式 .
(1)某烷烃1.16克与氧气完全燃烧,生成二氧化碳3.52克,通过计算确定该烃的分子式.
(2)标准状况下,体积为1.12L的含碳原子为n 和n+2个的两种气态烷烃的混合物质量为1.8克,试通过计算确定两种气态烷烃各是
(3)分子中含有31个共价键的烷烃D为
(4)室温下相对分子质量最大的气态烷烃F为
(5)写出甲苯的一氯取代有机产物的结构简式
考点:有关有机物分子式确定的计算,有机化合物中碳的成键特征
专题:有机化学基础
分析:(1)烷烃的通式为CnH2n+2,根据该烷烃的质量及生成二氧化碳的质量确定其分子式;
(2)根据n=
计算出混合烃的物质的量,然后计算出两种烃的平均摩尔质量,最后通过讨论确定烷烃的组成;
(3)烷烃的通式为CnH2n+2,烷烃中含有共价键数目为:n-1+2n+2=3n+1;
(4)室温下相对分子量最大的气态烷烃为新戊烷;
(5)氯原子可以取代甲基、甲基的邻位、间位和对位H原子,总共有4种同分异构体.
(2)根据n=
| V |
| Vm |
(3)烷烃的通式为CnH2n+2,烷烃中含有共价键数目为:n-1+2n+2=3n+1;
(4)室温下相对分子量最大的气态烷烃为新戊烷;
(5)氯原子可以取代甲基、甲基的邻位、间位和对位H原子,总共有4种同分异构体.
解答:
解:(1)设该烷烃的分子式为CnH2n+2,则该烷烃完全燃烧生成二氧化碳的质量为:
×n×44g/mol=3.52g,解得:n=4,该烷烃为丁烷,分子式为:C4H10,
故答案为:C4H10;
(2)标准状况下1.12L气体的物质的量为:n=
=0.05mol,该混合烃的平均摩尔质量为:
=36g/mol,在标况下为气体,则n和n+2都≤4,即n≤2;当n=1时,原则烷烃为甲烷、另一种为丙烷,甲烷的摩尔质量为16,丙烷的摩尔质量为44,满足条件;当n=2时,两种烃分别为乙烷、丁烷,乙烷的分子量为30、丁烷的分子量为58,也满足条件,
所以该两种气态烷烃可能为:CH4与C3H8或C2H6与C4H10,
故答案为:CH4与C3H8或C2H6与C4H10;
(3)烷烃的通式为CnH2n+2,该烷烃分子中碳原子形成了n-1g碳碳共价键,氢原子形成了2n+2个碳氢共价键,总共含有共价键数目为:n-1+2n+2=3n+1=31,解得:n=10,该烃的分子式为:C10H22,
故答案为:C10H22;
(4)新戊烷是常温下相对分子量最大的烷烃,其分子式为:C5H12,
故答案为:C5H12;
(5)甲苯的一氯代物总共有4种,分别为: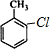 、
、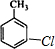 、
、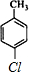 、
、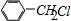 ,
,
故答案为: 、
、 、
、 、
、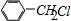 .
.
| 1.16g |
| (14n+2)g/mol |
故答案为:C4H10;
(2)标准状况下1.12L气体的物质的量为:n=
| 1.12L |
| 22.4L/mol |
| 1.8g |
| 0.05mol |
所以该两种气态烷烃可能为:CH4与C3H8或C2H6与C4H10,
故答案为:CH4与C3H8或C2H6与C4H10;
(3)烷烃的通式为CnH2n+2,该烷烃分子中碳原子形成了n-1g碳碳共价键,氢原子形成了2n+2个碳氢共价键,总共含有共价键数目为:n-1+2n+2=3n+1=31,解得:n=10,该烃的分子式为:C10H22,
故答案为:C10H22;
(4)新戊烷是常温下相对分子量最大的烷烃,其分子式为:C5H12,
故答案为:C5H12;
(5)甲苯的一氯代物总共有4种,分别为:
 、
、 、
、 、
、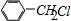 ,
,故答案为:
 、
、 、
、 、
、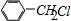 .
.
点评:本题考查了有机物分子式、结构简式的确定、同分异构体的书写,题目难度中等,注意掌握确定有机物分子式、结构简式的方法,明确同分异构体的概念及书写原则;试题侧重烷烃知识的考查,注意掌握烷烃的通式、分子组成及成键特点.

练习册系列答案
相关题目
已知次氯酸分子的结构式为H-O-Cl,下列有关说法正确的是( )
| A、O原子发生sp杂化 |
| B、O原子与H、Cl都形成σ键 |
| C、该分子为直线型分子 |
| D、该分子Cl原子显-1价 |
 氢气是一种新型的绿色能源,又是一种重要的化工原料.
氢气是一种新型的绿色能源,又是一种重要的化工原料.