题目内容
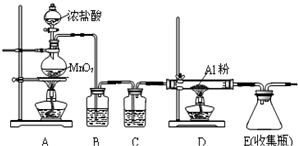
下列实验装置图正确的是( )
A.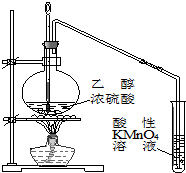 实验室制备并检验乙烯 | B.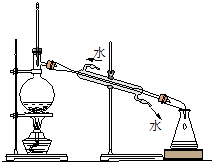 石油分馏 |
C.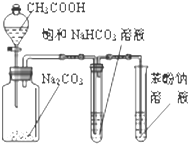 验证醋酸、碳酸、苯酚酸性强弱 | D.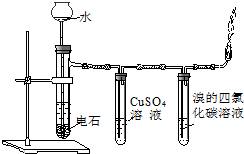 实验室制乙炔 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.乙醇能被酸性高锰酸钾溶液氧化;
B.冷凝管中下口为进水口、上口为出水口;
C.强酸能和弱酸盐反应生成弱酸;
D.滴加水的仪器应该用分液漏斗.
B.冷凝管中下口为进水口、上口为出水口;
C.强酸能和弱酸盐反应生成弱酸;
D.滴加水的仪器应该用分液漏斗.
解答:
解:A.乙醇具有挥发性,加热促进乙醇挥发,所以制取的乙烯中含有乙醇,乙醇也能被酸性高锰酸钾溶液氧化导致酸性高锰酸钾溶液褪色,从而影响乙烯的检验,所以在检验乙烯之前要出去乙醇,故A错误;
B.馏分温度较高,如果急剧冷却会导致冷凝管炸裂而易产生安全事故,所以冷凝管中的水从下口进、上口出,故B错误;
C.乙酸和碳酸钠反应生成二氧化碳,乙酸易挥发,导致二氧化碳中含有乙酸,用饱和碳酸氢钠溶液除去乙酸,二氧化碳和苯酚钠溶液反应生成苯酚和碳酸氢钠,所以该装置能检验醋酸、碳酸、苯酚酸性强弱,故C正确;
D.电石和水反应较剧烈,且电石和水反应生成氢氧化钙微溶物,氢氧化钙易堵塞长颈漏斗,为控制反应速率,应该用分液漏斗,故D错误;
故选C.
B.馏分温度较高,如果急剧冷却会导致冷凝管炸裂而易产生安全事故,所以冷凝管中的水从下口进、上口出,故B错误;
C.乙酸和碳酸钠反应生成二氧化碳,乙酸易挥发,导致二氧化碳中含有乙酸,用饱和碳酸氢钠溶液除去乙酸,二氧化碳和苯酚钠溶液反应生成苯酚和碳酸氢钠,所以该装置能检验醋酸、碳酸、苯酚酸性强弱,故C正确;
D.电石和水反应较剧烈,且电石和水反应生成氢氧化钙微溶物,氢氧化钙易堵塞长颈漏斗,为控制反应速率,应该用分液漏斗,故D错误;
故选C.
点评:本题考查了化学实验方案评价,明确实验原理及物质性质是解本题关键,注意从物质的性质、实验的可行性、评价性、实验原理等方面对实验装置进行评价,注意C中在检验二氧化碳和苯酚钠反应前要除去乙酸,为易错点.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
已知次氯酸分子的结构式为H-O-Cl,下列有关说法正确的是( )
| A、O原子发生sp杂化 |
| B、O原子与H、Cl都形成σ键 |
| C、该分子为直线型分子 |
| D、该分子Cl原子显-1价 |
除去NaHCO3溶液中的少量杂质Na2CO3,所用试剂或方法是( )
| A、加热 |
| B、Ca(OH)2溶液 |
| C、通入过量的CO2 |
| D、NaOH溶液 |
已知:①CO(g)+1/2O2(g)=CO2(g)△H1=-283.0kJ/mol
②H2(g)+1/2O2(g)=H2O(l)△H2=-285.8kJ/mol
③C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H3=-1370kJ/mol.
则2CO(g)+4H2(g)=H2O(l)+C2H5OH(l)的△H为( )
②H2(g)+1/2O2(g)=H2O(l)△H2=-285.8kJ/mol
③C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H3=-1370kJ/mol.
则2CO(g)+4H2(g)=H2O(l)+C2H5OH(l)的△H为( )
| A、-339.2 kJ/mol |
| B、-1983.8kJ/mol |
| C、+518.2kJ/mol |
| D、-801.2kJ/mol |
苯环实际上不具有碳碳单键和双键的简单交替结构,可以作为证据的事实有( )
| A、苯的间位二元取代物只有-种 |
| B、苯的邻位二元取代物只有一种 |
| C、苯不能使酸性KMnO4溶液褪色 |
| D、苯能在加热和催化剂存在的条件下与氯气加成生成环已烷 |

 官能团名称
官能团名称


