题目内容
3.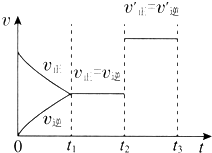 如图表示一定条件下N2+3H2?2NH3的反应速率和时间的关系,其中t1是达到平衡需要的时间,t2~t3是改变一个条件后出现的情况,则该条件可能是( )
如图表示一定条件下N2+3H2?2NH3的反应速率和时间的关系,其中t1是达到平衡需要的时间,t2~t3是改变一个条件后出现的情况,则该条件可能是( )| A. | 加压 | B. | 升温 | C. | 加入催化剂 | D. | 增大反应物浓度 |
分析 N2+3H2?2NH3的反应是气体体积减小的反应,其中t1是达到平衡需要的时间,t2~t3是改变一个条件后出现的情况正逆反应速率始终相同,但比原平衡状态反应速率大,说明是加入了催化剂,据此分析.
解答 解:N2+3H2?2NH3的反应是气体体积减小的反应,改变压强、温度、浓度对化学平衡都有影响,t1是达到平衡需要的时间,t2~t3是改变一个条件后出现的情况正逆反应速率始终相同,但比原平衡状态反应速率大,催化剂能改变化学反应速率,但不改变化学平衡,平衡不变,所以加入催化剂增大反应速率,不改变化学平衡,符合图中变化,故选C.
点评 本题考查了化学反应速率、化学平衡的影响因素分析,主要是图象中反应速率变化的特征判断,掌握基础是解题关键,题目难度不大.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
15.某有机物的分子式为C3H7O2N,关于它的叙述不正确的是( )
| A. | 该分子可能是天然蛋白质水解的产物 | |
| B. | 该分子核磁共振氢谱图可能有两个吸收峰,且面积之比为1:6 | |
| C. | 该分子只有2种同分异构体 | |
| D. | 分子中可能含有个一个羟基 |
11.下列关于热化学反应的描述中正确的是( )
| A. | CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的△H=+2×283.0kJ/mol | |
| B. | HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ba(OH)2反应的中和热△H=2×(-57.3)kJ/mol | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 已知反应H2S(g)+a O2(g)═X+c H2O(l)△H,若△H表示该反应的燃烧热,则X为SO2(g) |
8.1g氢气完全燃烧生成液态水放出142.9kJ的热量,表示该反应的热化学方程式为( )
| A. | 2H2+O2→2H2O+571.6 kJ | B. | 2H2(g)+O2(g)→2H2O(1)+142.9 kJ | ||
| C. | 2H2O(g)+O2(g)→2H2O(g)+571.6 kJ | D. | H2(g)+$\frac{1}{2}$O2(g)→H2O(1)+285.8 kJ |
15.某学生的实验报告所列出的下列数据中合理的是( )
| A. | .用10mL量筒量取7.28mL稀盐酸 | |
| B. | .用托盘天平称量25.50g NaCl | |
| C. | 用25mL滴定管做中和滴定时,用去某浓度的碱溶液21.60mL | |
| D. | 用广泛pH试纸测得某溶液的pH为2.7 |
12.下列关于维生素的说法不正确的是( )
| A. | 胡萝卜等蔬菜和鱼肝油中维生素C的量较高 | |
| B. | 维生素C能预防坏血病,具有较强的还原性,可将I2、Fe3+还原 | |
| C. | 维生素A难溶于水(脂溶性维生素)、维生素C易溶于水(水溶性维生素) | |
| D. | 维生素不提供能量,人体对它的需求量很小 |
13.下列有关物质性质的说法正确的是( )
| A. | 硫是一种黄色晶体,易溶于水 | |
| B. | 钠是一种银白色金属,熔点较高,硬度较大 | |
| C. | 二氧化硫是一种无色、无味的有毒气体 | |
| D. | 二氧化氮石红棕色、有刺激性气味的有毒气体 |