题目内容
1.X、Y、Z、W为短周期主族元素,X原子M层有1个电子,Y原子最外层电子数为为最内层电子数的2倍,Z元素的最高化合价为最低负化合价绝对值的3倍.Z、W同周期,W的 原子半径小于Z.下列叙述正确的是( )| A. | 原子半径由大到小的顺序:Z、X、Y | |
| B. | 元素非金属性由强到弱的顺序:W、Z、Y | |
| C. | 简单气态氢化物的稳定性强弱顺序:Z>W | |
| D. | W分别与X、Y形成的化合物化学键类型相同 |
分析 X、Y、Z、W为短周期主族元素,X原子M层有1个电子,应为Na元素,Y原子最外层电子数为最内层电子数的2倍,应为C或Si元素,Z元素的最高化合价为最低化合价绝对值的3倍,应为S元素,Z、W同周期,W的原子半径小于Z,则W为Cl元素,以此解答该题.
解答 解:X、Y、Z、W为短周期主族元素,X原子M层有1个电子,应为Na元素,Y原子最外层电子数为最内层电子数的2倍,应为C或Si元素,Z元素的最高化合价为最低化合价绝对值的3倍,应为S元素,Z、W同周期,W的原子半径小于Z,则W为Cl元素,
A.Na、S位于同一周期,Na为短周期原子半径最大的元素,故A错误;
B.同周期元素从左到右元素的非金属性逐渐增强,非金属性Cl>S>Si(C),故B正确;
C.非金属性Cl>S,元素的非金属性越强,对应的氢化物越稳定,故C错误;
D.W分别与X、Y形成的化合物分别为离子化合物、共价化合物,化学键类型不同,故D错误;
故选B.
点评 本题考查原子结构与元素周期律的关系,为高频考点,把握原子结构的关系推断各元素为解答的关键,注意元素周期律的应用,题目难度不大.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
12.下列有关说法正确的是( )
| A. | 铁在熔融状态下能导电,所以铁是电解质 | |
| B. | 氯化氢在熔融状态下不导电,所以氯化氢是非电解质 | |
| C. | 氯气的水溶液能导电,所以氯气是电解质 | |
| D. | 电解质和非电解质都是纯净物 |
9.非金属性最弱的元素是( )
| A. | C | B. | Si | C. | S | D. | Cl |
16.元素周期律揭示了元素间的递变规律,下列递变规律正确的是( )
| A. | ⅣA族元素氢化物沸点:SiH4>CH4,所以ⅤA族元素氢化物沸点:PH3>NH3 | |
| B. | 第二周期元素氢化物稳定性:HF>H2O,第三周期元素氢化物稳定性:HCl>H2S | |
| C. | ⅦA族元素的非金属性:F>Cl,所以ⅦA族元素氢化物的酸性:HF<HCl | |
| D. | 镁比铝活泼,工业上用电解熔融氧化铝制铝,所以工业上也用电解熔融氧化镁制镁 |
6.已知某原电池中某一极的电极反应式为Cu-2e-=Cu2+,则另一极的电极反应式可能是( )
| A. | H2-2e-═2H+ | B. | 2H++2e-═H2 | C. | Fe2++2e-═Fe | D. | 2Ag++2e-═2Ag |
13.下列有机物的命名正确的是( )
| A. | 二溴乙烷:CH2BrCH2Br | B. | 3-乙基-1-丁烯: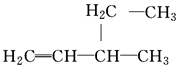 | ||
| C. | 2-甲基-2,4-己二烯: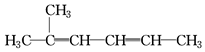 | D. | 2,2,3-三甲基戊烷: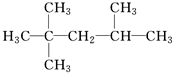 |
10.下列图象分别表示有关反应的反应过程与能量变化的关系,下列说法中正确的是( )
| A. | 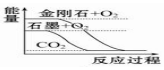 石墨转变为金刚石是吸热反应 | B. | 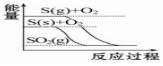 相同条件下等质量S(g)比S(s)的能量低 | ||
| C. | 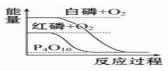 白磷比红磷稳定 | D. | 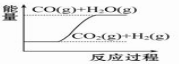 CO(g)+H2O(g)═CO2(g)+H2(g)是吸热反应 |
11.如图是一些常见的有机物的转化关系.下列说法错误的是( )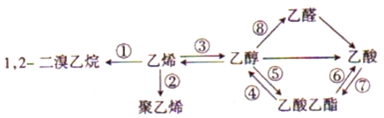

| A. | 反应①、③均属于加成反应 | B. | 乙酸与甲酸甲酯互为同分异构体 | ||
| C. | 乙醇溶液可除去暖瓶中的水垢 | D. | 反应④、⑤、⑥、⑦均属于取代反应 |