题目内容
2.(NH4)2PtCl6晶体受热分解,生成氮气、氯化氢、氯化铵和金属铂.在此分解反应中,还原产物与氧化产物的物质的量之比是( )| A. | 2:3 | B. | 1:3 | C. | 4:3 | D. | 3:2 |
分析 反应中只有N元素的化合价升高,由-3价升高为0价,氧化产物为氮气;Pt元素的化合价降低,由+4价降低为0价,还原产物为Pt,令Pt、氮气的物质的量分别为xmol、ymol,利用电子转移守恒计算.
解答 解:反应中只有N元素的化合价升高,由-3价升高为0价,氧化产物为氮气;Pt元素的化合价降低,由+4价降低为0价,还原产物为Pt,
令Pt、氮气的物质的量分别为xmol、ymol,则:
ymol×2×3=xmol×4
解得x:y=3:2,
故选D.
点评 本题考查氧化还原反应的计算,难度中等,利用氧化还原反应反应中电子守恒的计算即可解答.

练习册系列答案
相关题目
12. (1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
A通常显+3价,A的电负性>B的电负性(填“>”、“<”或“=”).
(2)紫外光的光子所具有的能量约为399kJ•mol-1.根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因紫外光具有的能量比蛋白质分子中重要的化学键C-C、C-N和C-S的键能都大,紫外光的能量足以使这些化学键断裂,从而破坏蛋白质分子.
组成蛋白质的最简单的氨基酸中的碳原子杂化类型是sp2和sp3.
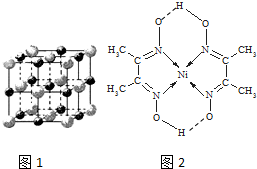
(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图1所示),其中3种离子晶体的晶格能数据如下表:
则该 4种离子晶体(不包括NaCl)熔点从高到低的顺序是:TiN>MgO>CaO>KCl.其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有12个.
(4)某配合物的分子结构如图2所示,其分子内不含有AC(填序号).
A、离子键 B、极性键 C、金属键 D、配位键 E、氢键 F、非极性键
(5)为消除温室效应的影响,科学家设计反应:CO2+4H2→CH4+2H2O以减小空气中CO2.若有1mol CH4生成,则有6molσ键和2molπ键断裂.
 (1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
(2)紫外光的光子所具有的能量约为399kJ•mol-1.根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因紫外光具有的能量比蛋白质分子中重要的化学键C-C、C-N和C-S的键能都大,紫外光的能量足以使这些化学键断裂,从而破坏蛋白质分子.
| 共价键 | C-C | C-N | C-S |
| 键能/kJ•mol-1 | 347 | 305 | 259 |
(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图1所示),其中3种离子晶体的晶格能数据如下表:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3401 |
(4)某配合物的分子结构如图2所示,其分子内不含有AC(填序号).
A、离子键 B、极性键 C、金属键 D、配位键 E、氢键 F、非极性键
(5)为消除温室效应的影响,科学家设计反应:CO2+4H2→CH4+2H2O以减小空气中CO2.若有1mol CH4生成,则有6molσ键和2molπ键断裂.
17. 往1.0mol•L-1KI溶液中加入固体I2,发生反应:I2(aq)+I- (aq)═I3-(aq)△H;I-的物质的量浓度c(I-)随温度T的变化曲线如图所示.已知反应第一次达到平衡时用时10s,则下列说法正确的是( )
往1.0mol•L-1KI溶液中加入固体I2,发生反应:I2(aq)+I- (aq)═I3-(aq)△H;I-的物质的量浓度c(I-)随温度T的变化曲线如图所示.已知反应第一次达到平衡时用时10s,则下列说法正确的是( )
 往1.0mol•L-1KI溶液中加入固体I2,发生反应:I2(aq)+I- (aq)═I3-(aq)△H;I-的物质的量浓度c(I-)随温度T的变化曲线如图所示.已知反应第一次达到平衡时用时10s,则下列说法正确的是( )
往1.0mol•L-1KI溶液中加入固体I2,发生反应:I2(aq)+I- (aq)═I3-(aq)△H;I-的物质的量浓度c(I-)随温度T的变化曲线如图所示.已知反应第一次达到平衡时用时10s,则下列说法正确的是( )| A. | 该反应的△H>0 | |
| B. | a、c两点对应的I-反应速率相等 | |
| C. | b点时0~10s I-的平均反应速率为0.04mol•L-1•s-1 | |
| D. | d点时该反应在对应温度下处于平衡状态 |
14.下列有关说法正确的是( )
| A. | 反应2Mg(s)+CO2(g)═2MgO(s)+C(s)能自发进行,则该反应的△H<0 | |
| B. | 铅蓄电池放电时反应为:PbO2+Pb+2H2SO4═2PbSO4+H2O,正、负极质量均减小 | |
| C. | 常温下,NH4Cl溶液加水稀释,$\frac{c(N{H}_{3}•{H}_{2}O)•c({H}^{+})}{c(N{H}_{4}^{+})}$不变 | |
| D. | 常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,充分搅拌后过滤,向洗净的沉淀中加稀盐酸,有气泡产生,说明常温下Ksp(BaCO3)<Ksp(BaSO4) |
11.下列不能用来鉴别乙烷和乙烯的方法是( )
| 选项 | 试剂或操作 | 鉴别方法 |
| A | 点燃 | 观察火焰 |
| B | 酸性高锰酸钾溶液 | 观察溶液颜色变化 |
| C | 水 | 观察水溶液 |
| D | 溴的四氯化碳溶液 | 观察溶液颜色变化 |
| A. | A | B. | B | C. | C | D. | D |
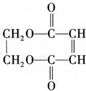 )可用于生产合成树脂、合成橡胶等.以丙烯为原料制备环酯J的合成路线如图:
)可用于生产合成树脂、合成橡胶等.以丙烯为原料制备环酯J的合成路线如图: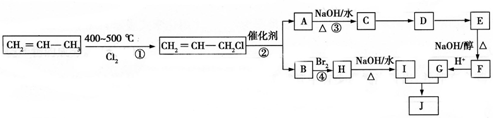
 ,G分子中含有的官能团是羧基和碳碳双键(填官能团名称).
,G分子中含有的官能团是羧基和碳碳双键(填官能团名称).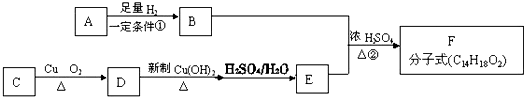
 或
或 或
或 ;
; .
.