题目内容
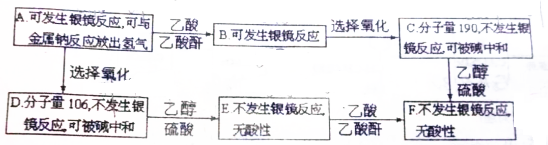
7.已知有机物A和C互为同分异构体且均为芳香族化合物,相互转化关系如图所示: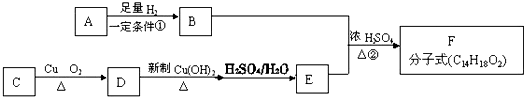
请回答下列问题:
(1)符合题意的有机物F的结构可能有3种,写出其中一种结构简式
 或
或 或
或 ;
;(2)指出反应反应类型①加成反应,②酯化反应或取代反应;
(3)写出发生下列转化的化学方程式:C→D
 .
.
分析 有机物A和C互为同分异构体且均为芳香族化合物,A、C中含有苯环,C能连续被氧化,则C为醇、D为醛、E为羧酸,A和氢气发生加成反应生成B,B和E能发生酯化反应生成F,A、C中碳原子相等,根据C原子守恒知,A、C中碳原子数都是7且B是一元醇、E是一元羧酸,E为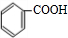 ,D为
,D为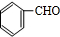 、C为
、C为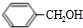 ,A、C为同分异构体,且A中含有羟基,A中还含有甲基,甲基和羟基可能位于邻位、间位或对位,所以A的结构简式可能为
,A、C为同分异构体,且A中含有羟基,A中还含有甲基,甲基和羟基可能位于邻位、间位或对位,所以A的结构简式可能为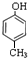
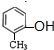 、
、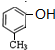 ,A发生加成反应生成B,B结构简式可能为
,A发生加成反应生成B,B结构简式可能为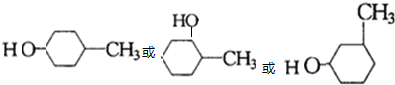 ,B、E发生酯化反应生成F,F结构简式为
,B、E发生酯化反应生成F,F结构简式为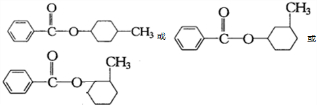 ,据此分析解答.
,据此分析解答.
解答 解:有机物A和C互为同分异构体且均为芳香族化合物,A、C中含有苯环,C能连续被氧化,则C为醇、D为醛、E为羧酸,A和氢气发生加成反应生成B,B和E能发生酯化反应生成F,A、C中碳原子相等,根据C原子守恒知,A、C中碳原子数都是7且B是一元醇、E是一元羧酸,E为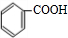 ,D为
,D为 、C为
、C为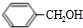 ,A、C为同分异构体,且A中含有羟基,A中还含有甲基,甲基和羟基可能位于邻位、间位或对位,所以A的结构简式可能为
,A、C为同分异构体,且A中含有羟基,A中还含有甲基,甲基和羟基可能位于邻位、间位或对位,所以A的结构简式可能为
 、
、 ,A发生加成反应生成B,B结构简式可能为
,A发生加成反应生成B,B结构简式可能为 ,
,
B、E发生酯化反应生成F,F结构简式为 或
或 或
或 ,
,
(1)通过以上分析知,F的结构简式可能为 或
或 或
或 ,共3种,
,共3种,
故答案为:3; 或
或 或
或 ;
;
(2)通过以上分析知,①②分别是加成反应、酯化反应或取代反应,
故答案为:加成反应;酯化反应或取代反应;
(3)C是苯甲醇,D是苯甲醛,苯甲醇被氧化生成苯甲醛,反应方程式为 ,
,
故答案为: ;
;
点评 本题考查有机物推断,以F为突破口采用逆向分析的方法进行推断,注意结合题给信息解答,同时考查学生获取信息、利用信息解答问题能力,熟练掌握醇、醛、羧酸、酯之间的转化及反应条件,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17. 现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
(1)已知液态BA3中与液态水类似,存在微弱的电离,写出其电离方程式2NH3?NH4++NH2-.
(2)B基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈纺锤形形.
(3)某同学根据上述信息,推断C基态原子的核外电子排布为,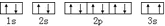 该同学所画的电子排布图违背了泡利原理.
该同学所画的电子排布图违背了泡利原理.
(4)G位于第ⅦB族d区,价电子排布式为3d54s2.
(5)DE3中心原子的杂化方式为sp3,用价层电子对互斥理论推测其空间构型为三角锥形.
(6)F元素的晶胞如图所示,若设该晶胞的密度为a g/cm3,阿伏加德罗常数为NA,F原子的摩尔质量为M g/mol,则F原子的半径为$\frac{\sqrt{3}}{4}$×$\root{3}{\frac{2M}{a{N}_{A}}}$ cm.
 现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别为 I1=738,I2=1451,I3=7733,I4=10540(单位:kJ/mol) |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(2)B基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈纺锤形形.
(3)某同学根据上述信息,推断C基态原子的核外电子排布为,
 该同学所画的电子排布图违背了泡利原理.
该同学所画的电子排布图违背了泡利原理.(4)G位于第ⅦB族d区,价电子排布式为3d54s2.
(5)DE3中心原子的杂化方式为sp3,用价层电子对互斥理论推测其空间构型为三角锥形.
(6)F元素的晶胞如图所示,若设该晶胞的密度为a g/cm3,阿伏加德罗常数为NA,F原子的摩尔质量为M g/mol,则F原子的半径为$\frac{\sqrt{3}}{4}$×$\root{3}{\frac{2M}{a{N}_{A}}}$ cm.
2.(NH4)2PtCl6晶体受热分解,生成氮气、氯化氢、氯化铵和金属铂.在此分解反应中,还原产物与氧化产物的物质的量之比是( )
| A. | 2:3 | B. | 1:3 | C. | 4:3 | D. | 3:2 |
12.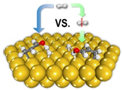 2013年《美国化学会志》发表了我国科学家对非均相催化加氢过程机理研究的成果,其原理如图.下列关于氢气的说法不正确的是( )
2013年《美国化学会志》发表了我国科学家对非均相催化加氢过程机理研究的成果,其原理如图.下列关于氢气的说法不正确的是( )
 2013年《美国化学会志》发表了我国科学家对非均相催化加氢过程机理研究的成果,其原理如图.下列关于氢气的说法不正确的是( )
2013年《美国化学会志》发表了我国科学家对非均相催化加氢过程机理研究的成果,其原理如图.下列关于氢气的说法不正确的是( )| A. | 由氢原子构成的氢气分子只有一种 | |
| B. | 通常情况下,气体中氢气的密度最小 | |
| C. | 氢气可用于生产盐酸、氨气等化工产品 | |
| D. | 目前,工业上不采用电解水的方法大量生产氢气 |
19.下列说法正确的是( )
| A. | 溶液、胶体、浊液三种分散系可用丁达尔效应进行区分 | |
| B. | △H<0且△S>0的反应可以自发进行 | |
| C. | 酸碱中和滴定实验中装标准液的滴定管未润洗,会造成所测结果偏低 | |
| D. | 钢铁吸氧腐蚀的负极反应为:O2+4e-+2H2O═4OH- |
16.设NA为阿伏加德罗常数,下列叙述正确的是(相对原子质量O-16 Na-23)( )
| A. | 25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| B. | 100 mL 1 mol•L-1的H2SO4溶液中含有0.1NA个H+ | |
| C. | 将4 g NaOH溶于100 g蒸馏水中,所得溶液物质的量浓度是0.1 mol•L-1 | |
| D. | 20g重水(D2O)所含的电子数为10NA |
 .
.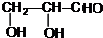 +2Ag(NH3)2OH$\stackrel{△}{→}$
+2Ag(NH3)2OH$\stackrel{△}{→}$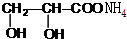 +2Ag↓+3NH3+H2O.
+2Ag↓+3NH3+H2O.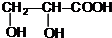 +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$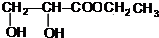 +H2O,属于取代反应(填反应类型).
+H2O,属于取代反应(填反应类型).