题目内容
5.下列关于材料的说法,不正确的是( )| A. | 不锈钢属于一种铁合金 | |
| B. | 纤维素是蚕丝的主要成分 | |
| C. | 水泥是生活中常见的硅酸盐材料 | |
| D. | 二氧化硅是制造光导纤维的主要原料 |
分析 A.不锈钢是钢的一种,是铁的合金;
B.蚕丝是天然纤维,主要成分是蛋白质;
C.三大传统硅酸盐产品是玻璃、陶瓷、水泥;
D.光导纤维是以纯净的二氧化硅晶体为原料制造的.
解答 解:A.不锈钢是铁合金,还含有抗腐蚀性很强的铬和镍,故A正确;
B.蚕丝属于天然纤维,主要成分是蛋白质,故B错误;
C.玻璃、陶瓷、水泥成分中含有硅酸盐属于硅酸盐材料,是生活中常见的硅酸盐材料,故C正确;
D.光导纤维传递光信号的原理是光的全反射,SiO2具有良好的光学效果材料,是制造光导纤维的主要原料,故D正确.
故选B.
点评 本题主要考查了合金、无机非金属材料、蚕丝的成分等,题目难度不大,注意制光导纤维的原料二氧化硅、蚕丝的成分是高频考点.

练习册系列答案
相关题目
15.下列说法不正确的是( )
| A. | 用焰色反应可鉴别NaCl和KCl | |
| B. | 氢氟酸可用于刻蚀玻璃,是利用SiO2酸性氧化物的性质 | |
| C. | 气体通过无水硫酸铜,粉末变蓝,证明原气体中含有水蒸气 | |
| D. | 在食品包装袋中放入硅胶防止食品变质,是利用硅胶的吸水性 |
13.下列关于Na2CO3溶液的说法,正确的是( )
| A. | 相同温度下,Na2C03溶液中水的电离程度比纯水的电离程度小 | |
| B. | 相同温度下,Na2C03溶液中滴加酚酞呈红色,NaHC03溶液中滴加酚酞颜色更深 | |
| C. | VLamoL/L的Na2C03溶液中,若C032-的数目为NA;则Na+的数目大于2NA | |
| D. | CaC03在饱和Na2C03溶液中的KSP比在纯水中的KSP小 |
20.在迎接“绿色校园”的主题活动中,小明同学提出下列倡议,不可采纳的是( )
| A. | 提倡绿色出行 | B. | 提倡使用无磷洗涤剂 | ||
| C. | 提倡使用一次性塑料袋 | D. | 提倡垃圾分类和回收利用 |
10.钢铁厂在冷轧过程中会产生高浓度酸性含铁废水,主要含有H+、Cl-、Fe2+、Fe3+等,其处理的主要工艺流程如下:
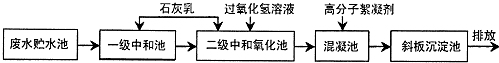
请回答:
(1)废水未经处理直接排放的危害是ab(填字母).
a腐蚀水利设施 b影响水生生物的自然生长
(2)石灰乳用于中和含铁废水中的酸,写出石灰乳与盐酸反应的化学方程式:Ca(OH)2+2HCl═CaCl2+2H2O.
(3)过氧化氧的主要作用是b(填字母).a还原剂 b氧化剂
(4)自来水厂常用漂白粉、液氯、二氧化氯、臭氧等作为消毒剂,杀灭水中的细菌.液氯注入水中后,能杀死水中细菌的物质是HClO(填化学式).
(5)污水处理中的主要化学方法有中和法、混凝法_、_沉淀法_、氧化还原法.
(6)某研究小组对钢铁厂高浓度酸性含铁废水进行监测时,取其样本稀释,测得有关数据如下:
稀释后的溶液中c(Fe2+)=0.12mol/L.

请回答:
(1)废水未经处理直接排放的危害是ab(填字母).
a腐蚀水利设施 b影响水生生物的自然生长
(2)石灰乳用于中和含铁废水中的酸,写出石灰乳与盐酸反应的化学方程式:Ca(OH)2+2HCl═CaCl2+2H2O.
(3)过氧化氧的主要作用是b(填字母).a还原剂 b氧化剂
(4)自来水厂常用漂白粉、液氯、二氧化氯、臭氧等作为消毒剂,杀灭水中的细菌.液氯注入水中后,能杀死水中细菌的物质是HClO(填化学式).
(5)污水处理中的主要化学方法有中和法、混凝法_、_沉淀法_、氧化还原法.
(6)某研究小组对钢铁厂高浓度酸性含铁废水进行监测时,取其样本稀释,测得有关数据如下:
| 离子 | H+ | Cl- | Fe2+ | Fe3+ |
| 浓度(mol•L)-1 | 0.16 | 0.94 | 0.18 |
14.I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?═?I3-(aq).测得不同温度下该反应的平衡常数如下表:
下列说法正确的是( )
| t/℃ | 5 | 15 | 25 | 35 | 50 |
| K | 1 000 | 850 | 690 | 625 | 400 |
| A. | 反应I2(aq)+I-(aq)?═?I3-(aq)的△H>0 | |
| B. | 利用该反应可以除去硫粉中少量的碘单质 | |
| C. | 在上述平衡体系中加入苯,平衡不移动 | |
| D. | 25℃时,向溶液中加入少量KI固体,平衡常数K小于690 |
15. 钠及其化合物在生产和生活中有广泛的应用.完成下列计算:
钠及其化合物在生产和生活中有广泛的应用.完成下列计算:
(1)钠铝合金可作核反应堆的载热介质.取1.46g的钠铝合金放入水中,合金全部溶解,放出1.12L氢气(标准状况),则该钠铝合金的化学式为Na2Al.
(2)NaCN是一种剧毒的化工原料,可用双氧水处理含NaCN的废液,发生反应的方程式为:NaCN+H2O2+H2O=NaHCO3+NH3.若处理含NaCN 4.90g的废液,需用15%的H2O221.65mL.(已知15% H2O2的密度是1.047g/mL)(保留2位小数)
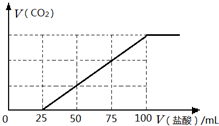
(3)向100mL NaOH溶液中通入一定量的CO2气体,充分反应后得到溶液A,再向A中逐滴加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示.试计算溶液A的溶质成份及其物质的量.
(4)常温下,称取不同氢氧化钠样品溶于水,加盐酸中和至pH=7,然后将溶液蒸干得氯化钠晶体,蒸干过程中产品无损失.
上述实验①②③所用氢氧化钠均不含杂质,且实验数据可靠.通过计算,分析和比较上表3组数据,给出结论.
 钠及其化合物在生产和生活中有广泛的应用.完成下列计算:
钠及其化合物在生产和生活中有广泛的应用.完成下列计算:(1)钠铝合金可作核反应堆的载热介质.取1.46g的钠铝合金放入水中,合金全部溶解,放出1.12L氢气(标准状况),则该钠铝合金的化学式为Na2Al.
(2)NaCN是一种剧毒的化工原料,可用双氧水处理含NaCN的废液,发生反应的方程式为:NaCN+H2O2+H2O=NaHCO3+NH3.若处理含NaCN 4.90g的废液,需用15%的H2O221.65mL.(已知15% H2O2的密度是1.047g/mL)(保留2位小数)
(3)向100mL NaOH溶液中通入一定量的CO2气体,充分反应后得到溶液A,再向A中逐滴加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示.试计算溶液A的溶质成份及其物质的量.
(4)常温下,称取不同氢氧化钠样品溶于水,加盐酸中和至pH=7,然后将溶液蒸干得氯化钠晶体,蒸干过程中产品无损失.
| 氢氧化钠质量(g) | 氯化钠质量(g) | |
| ① | 2.40 | 3.51 |
| ② | 2.32 | 2.34 |
| ③ | 3.48 | 3.51 |
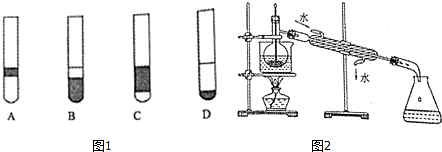
 下列装置中,a5是铁电极,其余为石墨电极,烧杯中液体体积均为100mL,放置一段时间后(溶质都有剩余),回答下列问题(不考虑溶液体积变化)
下列装置中,a5是铁电极,其余为石墨电极,烧杯中液体体积均为100mL,放置一段时间后(溶质都有剩余),回答下列问题(不考虑溶液体积变化)