题目内容
15.下列说法不正确的是( )| A. | 用焰色反应可鉴别NaCl和KCl | |
| B. | 氢氟酸可用于刻蚀玻璃,是利用SiO2酸性氧化物的性质 | |
| C. | 气体通过无水硫酸铜,粉末变蓝,证明原气体中含有水蒸气 | |
| D. | 在食品包装袋中放入硅胶防止食品变质,是利用硅胶的吸水性 |
分析 A.Na和K元素的焰色反应现象不同;
B.酸性氧化物能与碱反应反应生成盐和水;
C.无水硫酸铜吸水变为CuSO4•5H2O,白色粉末变蓝,可证明原气体中含有水蒸气;
D.硅胶易吸水.
解答 解:A.Na和K元素的焰色反应现象不同,可将二者鉴别,故A正确;
B.氢氟酸能与二氧化硅反应生成四氟化硅气体,不是酸性氧化物的性质,故B错误;
C.气体通过无水硫酸铜,粉末变蓝,则发生反应:CuSO4+5H2O═CuSO4•5H2O,可证明原气体中含有水蒸气,故C正确;
D.硅胶易吸水,能防止食品变质,故D正确.
故选B.
点评 本题考查焰色反应、酸性氧化物、脱水性和干燥剂,题目难度不大,注意酸性氧化物不能与酸反应,氢氟酸能与二氧化硅反应,不是酸性氧化物的性质.

练习册系列答案
相关题目
3.下列化合物中同分异构体数目最少的是( )
| A. | C2H4O2 | B. | C3H8O | C. | C3H7Cl | D. | C5H12 |
10.下表是某矿泉水的部分标签说明

则该饮用水中还可能较大量存在的离子是( )

则该饮用水中还可能较大量存在的离子是( )
| A. | OH- | B. | Ag+ | C. | Na+ | D. | Ba2+ |
20.常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,下列说法正确的是( )
| A. | HA为强酸 | B. | 该混合液pH=7 | ||
| C. | 该混合溶液中:c(Na+)>c(A-)>c(OH-)>c(H+) | D. | 该混合溶液中:c(A-)+c(OH-)=c(Na+)+c(H+) |
7.按电子排布,可以把周期表中的元素划分成几个区( )
| A. | 4个 | B. | 5个 | C. | 6个 | D. | 7个 |
4.室温下,下列各组离子在指定溶液中,一定能大量共存的是( )
| A. | pH=1的溶液中:Na+、Fe3+、NO3-、I- | |
| B. | 水电离出的c(H+)=1×10-12mol•L-1的溶液中:K+、Al3+、Cl-、SO42- | |
| C. | c(AlO2-)=0.1 mol•L-1的溶液中:Na+、K+、HCO3-、Cl- | |
| D. | 加入KSCN溶液显红色的溶液:K+、NH4+、Cl-、NO3- |
5.下列关于材料的说法,不正确的是( )
| A. | 不锈钢属于一种铁合金 | |
| B. | 纤维素是蚕丝的主要成分 | |
| C. | 水泥是生活中常见的硅酸盐材料 | |
| D. | 二氧化硅是制造光导纤维的主要原料 |
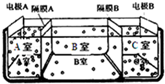 水是一种重要的自然资源,是人类赖以生存不可缺少的物质.请回答下列问题:
水是一种重要的自然资源,是人类赖以生存不可缺少的物质.请回答下列问题: