题目内容
由电解法获得的粗铝中含一定量的金属钠和氢气,这些杂质可采用吹气精炼法除去,产生的尾气经处理后可用于钢材镀铝.工艺流程如图所示:(注:NaCl熔点为801℃;AlCl3在181℃升华)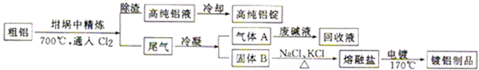
(1)精炼前,需清除坩埚表面的氧化铁和石英砂,防止精炼时它们分别与铝发生置换反应产生新的杂质,其中石英砂与铝反应的化学方程式为 .
(2)将Cl2连续通入坩埚中的粗铝熔体,杂质随气泡上浮除去.气泡的主要成分除Cl2外还含有 ;固态杂质粘附于气泡上,在熔体表面形成浮渣,浮渣中肯定存在 .
(3)在用废碱液处理气体A的过程中,所发生反应的离子方程式为 .
(4)镀铝电解池中,熔融盐电镀液中铝元素和氮元素主要以AlCl4-形式存在,铝电极的主要电极反应式为 .

(1)精炼前,需清除坩埚表面的氧化铁和石英砂,防止精炼时它们分别与铝发生置换反应产生新的杂质,其中石英砂与铝反应的化学方程式为
(2)将Cl2连续通入坩埚中的粗铝熔体,杂质随气泡上浮除去.气泡的主要成分除Cl2外还含有
(3)在用废碱液处理气体A的过程中,所发生反应的离子方程式为
(4)镀铝电解池中,熔融盐电镀液中铝元素和氮元素主要以AlCl4-形式存在,铝电极的主要电极反应式为
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:粗铝700°C通入氯气在坩埚中精炼,将Cl2连续通入坩埚中的粗铝熔体,杂质随气泡上浮除去.气泡的主要成分除Cl2外还含有H2、HCl、AlCl3,除渣得到高纯铝液和尾气,高纯铝液冷却得到高纯铝锭,尾气冷凝得到气体A为Cl2,废碱液回收得到回收液;B固体加入氯化钠氯化钾加热得到熔融盐电镀得到镀铝制品;
(1)根据氧化铁和石英砂(主要成分是二氧化硅)能分别与铝发生置换反应来书写方程式;
(2)根据题中信息:NaCl熔点为801℃;AlCl3在181℃升华,在结合物质之间的反应来分析;
(3)酸性气体能和强碱反应,用烧碱来处理尾气;
(4)电镀池中镀件金属作阳极,金属发生氧化反应;
(1)根据氧化铁和石英砂(主要成分是二氧化硅)能分别与铝发生置换反应来书写方程式;
(2)根据题中信息:NaCl熔点为801℃;AlCl3在181℃升华,在结合物质之间的反应来分析;
(3)酸性气体能和强碱反应,用烧碱来处理尾气;
(4)电镀池中镀件金属作阳极,金属发生氧化反应;
解答:
解:(1)精炼前,需清除坩埚表面的氧化铁和石英砂,防止精炼时它们分别与铝发生置换反应产生新的杂质,其中石英砂与铝反应的化学方程式为:4Al+3SiO2
3Si+2Al2O3,故答案为:4Al+3SiO2
3Si+2Al2O3;
(2)粗铝含有一定量的金属钠和氢气,钠、铝和氯气反应生成了氯化钠和氯化铝,氢气和氯气发生反应生成氯化氢,其中氯化钠熔点为801℃,较高,是固态杂质随气泡上浮,气泡的主要成分除Cl2外还含有H2、HCl、AlCl3,故答案为:H2、HCl、AlCl3;NaCl;
(3)A中有氯气以及氯化氢,均能和烧碱反应,用于尾气处理,实质为:Cl2+2OH-=Cl-+ClO-+H2O,H++OH-=H2O;
故答案为:Cl2+2OH-=Cl-+ClO-+H2,OH++OH-=H2O;
(4)电镀池中镀件金属铝作阳极,金属铝失电子发生氧化反应,Al-3e-+4Cl-═AlCl4-;
故答案为:Al-3e-+4Cl-═AlCl4-;
| ||
| ||
(2)粗铝含有一定量的金属钠和氢气,钠、铝和氯气反应生成了氯化钠和氯化铝,氢气和氯气发生反应生成氯化氢,其中氯化钠熔点为801℃,较高,是固态杂质随气泡上浮,气泡的主要成分除Cl2外还含有H2、HCl、AlCl3,故答案为:H2、HCl、AlCl3;NaCl;
(3)A中有氯气以及氯化氢,均能和烧碱反应,用于尾气处理,实质为:Cl2+2OH-=Cl-+ClO-+H2O,H++OH-=H2O;
故答案为:Cl2+2OH-=Cl-+ClO-+H2,OH++OH-=H2O;
(4)电镀池中镀件金属铝作阳极,金属铝失电子发生氧化反应,Al-3e-+4Cl-═AlCl4-;
故答案为:Al-3e-+4Cl-═AlCl4-;
点评:本题考查了物质分离提纯的流程分析判断,物质性质和试剂作用于产物的判断是解题关键,是一道有关金属的工业制备知识题目,考查角度广,难度较大.

练习册系列答案
相关题目
下列关于胶体的叙述不正确的是( )
| A、胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9~10-7m之间 |
| B、胶体是一种比较均一、稳定的混合物 |
| C、用平行光照射NaCl溶液和Fe(OH)3胶体时,产生的现象相同 |
| D、Al(OH)3胶体能够吸附水中悬浮的固体颗粒沉降,达到净水目的 |
下列有关实验中安全操作或事故处理中正确的是 ( )
| A、将100g水倒入100g 98% 硫酸溶液中配制成49% 的硫酸溶液 |
| B、给试管里的液体加热时,液体体积不得超过试管容积的1/3 |
| C、使用胶头滴管时,应将滴管尖嘴伸进试管内,以免液体外流 |
| D、不小心将浓硫酸洒到桌面上,应先用抹布擦,再用大量水冲洗 |
 0.100 0mol/L的KOH标准溶液滴定未知浓度盐酸,其操作可分解为如下几步:
0.100 0mol/L的KOH标准溶液滴定未知浓度盐酸,其操作可分解为如下几步:
