题目内容
已知某溶液中Cl-、Br-、I-的离子数之比为1:2:3,要使其溶液中的Cl-、Br-、I-的离子数之比变为1:1:1,则通入Cl2的分子数与原溶液中I-离子数之比为( )
| A、1:2 | B、1:3 |
| C、1:6 | D、3:1 |
考点:氧化还原反应的计算
专题:氧化还原反应专题
分析:还原性:I->Br->Cl-,通入一定量的Cl2,比值变为1:1:1,说明溶液中剩余I-,则只氧化I-,Br-的物质的量不变,假定Br-为2mol,根据离子物质的量变化计算通入的氯气的物质的量,据此计算解答.
解答:
解:还原性:I->Br->Cl-,通入一定量的Cl2,比值变为1:1:1,说明溶液中剩余I-,
设Cl-、Br-、I-三者物质的量分别是1mol、2mol、3mol,则反应后分别为2mol、2mol、2mol,则增加Cl-1mol,I-减少1mol,
由方程式2I-+Cl2=I2+2Cl-可知,参加反应的Cl2为0.5mol,
则通入Cl2的分子数与原溶液中I-离子数之比为0.5mol:3mol=1:6,
故选C.
设Cl-、Br-、I-三者物质的量分别是1mol、2mol、3mol,则反应后分别为2mol、2mol、2mol,则增加Cl-1mol,I-减少1mol,
由方程式2I-+Cl2=I2+2Cl-可知,参加反应的Cl2为0.5mol,
则通入Cl2的分子数与原溶液中I-离子数之比为0.5mol:3mol=1:6,
故选C.
点评:本题考查卤素单质及其化合物的性质、化学计算等,难度不大,注意比较物质的氧化性、还原性的强弱,根据所发生的反应结合化学方程式计算.

练习册系列答案
相关题目
下列除去杂质或鉴别方法正确的是( )
| A、除去乙烷中少量的乙烯:光照条件下通入Cl2,使乙烯转化成液态二氯乙烷而与乙烷分离 |
| B、除去乙酸乙酯中少量的乙酸:用氢氧化钠溶液洗涤,分液、干燥、蒸馏 |
| C、可以用溴水鉴别乙醇、甲苯、四氯化碳、植物油 |
| D、只用银氨溶液就可以鉴别淀粉是否完全水解 |
下列物质分离、提纯能达到目的是( )
| A、可用过滤分离FeCl3溶液和Fe3O4胶体的混合物 |
| B、除去铜粉中混有的少量铁粉应先加足量氯化铁溶液,然后过滤 |
| C、用浓硫酸吸收二氧化硫中混有少量SO3气体 |
| D、除去NaCl晶体中少量KNO3,可以将混合物制成热的饱和溶液,然后冷却结晶,过滤 |
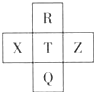 元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )| A、非金属性:Z<T<X |
| B、R与Q原子核外电子数相差26 |
| C、气态氢化物稳定性:R<T<Q |
| D、最高价氧化物的水化物的酸性:X>T |
下列离子方程式错误的是( )
| A、向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O |
| B、酸性介质中KMnO4氧化H2O2:2MnO4-+5H2O2 +6H+═2Mn2++5O2↑+8H2O |
| C、等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH-═Mg(OH)2↓ |
| D、铅酸蓄电池充电时的正极反应:PbSO4+2H2O-2e-═PbO2+4H++SO42- |
下列关于某些问题的说法中,正确的是( )
| A、禁用含铅汽油是为了提高汽油的燃烧效率 |
| B、甲醇与乙醇是同系物,所以酒中含有甲醇是允许饮用的 |
| C、甲醛的水溶液可用于防腐,所以可以食用用甲醛浸泡过的动物内脏 |
| D、“白色污染”是指聚乙烯等塑料垃圾 |
下列各组混合物,可以用分液漏斗分离的是( )
| A、甲苯和水 | B、甲苯和苯 |
| C、溴乙烷与水 | D、苯与溴乙烷 |