题目内容
下列各组混合物,可以用分液漏斗分离的是( )
| A、甲苯和水 | B、甲苯和苯 |
| C、溴乙烷与水 | D、苯与溴乙烷 |
考点:物质的分离、提纯的基本方法选择与应用
专题:实验题
分析:可以用分液漏斗分离,则选项中的物质混合分层,结合物质的溶解性来解答.
解答:
解:A.甲苯和水混合分层,可利用分液漏斗分离,故A选;
B.甲苯和苯相互溶解,不分层,不能用分液漏斗分离,故B不选;
C.溴乙烷与水混合分层,可利用分液漏斗分离,故C选;
D.苯与溴乙烷相互溶解,不分层,不能用分液漏斗分离,故D不选;
故选AC.
B.甲苯和苯相互溶解,不分层,不能用分液漏斗分离,故B不选;
C.溴乙烷与水混合分层,可利用分液漏斗分离,故C选;
D.苯与溴乙烷相互溶解,不分层,不能用分液漏斗分离,故D不选;
故选AC.
点评:本题考查混合物分离提纯方法及选择,为高频考点,把握分层的液体可利用分液漏斗分离为解答的关键,注意常见物质的溶解性及相似相容原理,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
已知某溶液中Cl-、Br-、I-的离子数之比为1:2:3,要使其溶液中的Cl-、Br-、I-的离子数之比变为1:1:1,则通入Cl2的分子数与原溶液中I-离子数之比为( )
| A、1:2 | B、1:3 |
| C、1:6 | D、3:1 |
下列关于元素周期律的叙述正确的是( )
| A、元素的性质随着原子序数的递增而呈周期性变化 |
| B、随着元素原子序数的递增,原子最外层电子数总是从1到8重复出现 |
| C、随着元素原子序数的递增,元素的最高化合价从+1到+7,最低化合价从-7到-1重复出现 |
| D、元素性质的周期性变化是指相对原子量的周期性变化、原子半径的周期性变化及元素主要化合价的周期性变化 |
下列各组中的性质比较,错误的是( )
| A、酸性:H2SiO3<H2SO4<HClO4 |
| B、碱性:NaOH>Mg(OH)2>Al(OH)3 |
| C、稳定性:HCl>H2S>PH3 |
| D、还原性:F->Cl->Br- |
已知还原性Fe2+>Br一,向100mLFeBr2溶液中通入标准状况下的C126.72L,C12全部被还原,测得溶液中c(Br-)=c(C1-),则原FeBr2溶液的物质的量浓度是( )
| A、1mol/L |
| B、2mol/L |
| C、3 mol/L |
| D、4 mol/L |
除去乙烷C2H6中混有的少量乙烯C2H4,选择方案合理是( )
| A、溴水、洗气 |
| B、高锰酸钾、洗气 |
| C、氢气、催化剂加成 |
| D、乙烷脱氢 |
下列元素性质的递变规律正确的是( )
| A、原子半径:Be<B<C<N |
| B、第一电离能:B<Be<Mg<Na |
| C、元素的电负性:O>N>S>P |
| D、气态氢化物的稳定性:NH3<CH4<PH3<SiH4 |
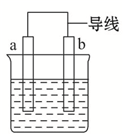 如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:
如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题: