题目内容
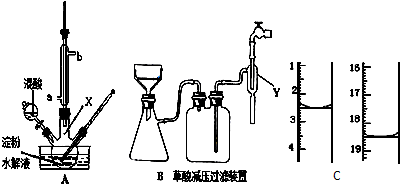
16.用硝酸氧化淀粉水解的产物(C6H12O6)可制得少量草酸,装置如图A所示(加热、搅拌和仪器固定装置均已略去):
已知硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O
C6H12O6+8HNO3→6CO2+8NO↑+10H2O
3H2C2O4+2HNO3→6CO2+2NO↑+4H2O
实验过程如下:
①将1:1的淀粉水乳液与少许硫酸(98%)加入烧杯中,
水浴加热至85℃~90℃,保持30min,然后逐渐将温度降至60℃左右;
②将一定量的淀粉水解液加入容器X中;
③控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2:1.5)溶液;
④反应3h左右,冷却,减压过滤后再重结晶得草酸晶体.
请回答下列问题:
(1)容器X的名称:三颈烧瓶.
(2)冷凝管水的进口是a(填a或b);冷凝管冷凝回流的主要物质是硝酸.
(3)实验中若混酸滴加过快,将导致草酸产量下降,其原因是由于温度过高、硝酸浓度过大,导致C6H12O6和H2C2O4进一步被氧化.
(4)该装置最大的一个缺点是缺少尾气处理装置.
(5)草酸重结晶的减压过滤装置如图B.仪器Y接在水龙头上,其作用是起抽气作用,使吸滤瓶、安全瓶中的压强减小.减压过滤的操作有:①将含晶体的溶液倒入漏斗;②将滤纸放入漏斗并用水湿润;③打开水龙头;④关闭水龙头;⑤拆下橡皮管.正确的顺序是②③①⑤④.
(6)将产品在恒温箱内约90℃以下烘干至恒重,得到二水合草酸.用KMnO4标准溶液滴定,该反应的离子方程式为:
2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O
称取该样品0.12g,加适量水完全溶解,然后用0.020mol•L-1的酸性KMnO4溶液滴定至终点(杂质不参与反应),此时溶液颜色由无色变为紫红色(或淡紫色).滴定前后滴定管中的液面读数如图C所示,则该草酸晶体样品中二水合草酸的质量分数为84%.
分析 (1)根据装置图可知其名称;
(2)冷凝水流向与蒸气流向逆向时冷凝效果最佳;硝酸易挥发;
(3)草酸具有还原性,硝酸能进一步氧化C6H12O6和H2C2O4;
(4)反应后生成的产物为一氧化氮、二氧化氮,为有毒气体,需要进行尾气处理;
(5)依据减压过滤的条件解答;依据减压过滤的正确操作排序解答;
(6)高锰酸钾为紫红色,过程中不需要加指示剂;在酸性条件下,高锰酸根离子能和草酸发生氧化还原反应生成二价锰离子、二氧化碳和水,根据反应计算.
解答 解:(1)容器X的名称为三颈烧瓶,故答案为:三颈烧瓶;
(2)冷凝水流向与蒸气流向逆向时冷凝效果最佳,所以应从a口进入;硝酸易挥发,所以需要进行冷凝,故答案为:a;硝酸;
(3)混酸为65%HNO3与98%H2SO4的混合液,混合液溶于水放热,温度高能加快化学反应,硝酸能进一步氧化H2C2O4成二氧化碳,
故答案为:由于温度过高、硝酸浓度过大,导致C6H12O6 和H2C2O4进一步被氧化;
(4)反应后生成的产物为一氧化氮、二氧化氮,为有毒气体,需要进行尾气处理,所以装置最大的一个缺点缺少尾气处理装置;
故答案为:缺少尾气处理装置;
(5)草酸重结晶的减压过滤装置如图B,通过仪器Y接在水龙头上,起抽气作用,使吸滤瓶、安全瓶中的压强减小;
减压过滤的操作为:②将滤纸放入漏斗并用水湿润;③打开水龙头;①将含晶体的溶液倒入漏斗;⑤拆下橡皮管;④关闭水龙头;
故答案为:起抽气作用,使吸滤瓶、安全瓶中的压强减小;②③①⑤④;
(6)高锰酸钾溶液为紫红色,当达到滴定终点时,再滴入高锰酸钾溶液时,淡紫色不再褪去,草酸钠(Na2C2O4)溶于稀硫酸中,然后用酸性高锰酸钾溶液进行滴定,离子方程式为:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O,n(KMnO4)=0.016L×0.0200mol•L-1=3.2×10-3mol,根据方程式可得:
2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O.
2 5
3.2×10-3mol 8×10-3mol
样品中二水合草酸的质量为m=8×10-3mol×126g/mol=8×126×10-3g=1.008g,
则该草酸晶体样品中二水合草酸的质量分数为$\frac{1.008g}{1.2g}$×100%=84%,
故答案为:无色;紫红色(或淡紫色);84%.
点评 本题考查了草酸的制取,把握实验的原理,熟练进行氧化还原计算是解答的关键,注意用结晶法分离固体混合物及其抽滤的实验操作,题目难度较大.

 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案| A. | $\frac{1}{\sqrt{a}}$ | B. | $\sqrt{a}$ | C. | $\frac{1}{2}$a | D. | $\frac{1}{\frac{1}{2}a}$ |
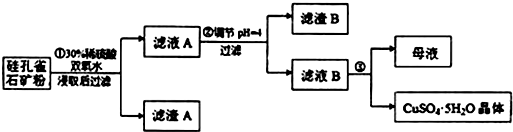
请回答下列问题:
(1)完成步骤①中稀硫酸与CuSiO3•2H2O发生反应的化学方程式
CuSiO3•2H2O+H2SO4═CuSO4+H4SiO4+H2O;
用离子方程式表示双氧水的作用2Fe2++H2O2+2H+═2Fe3++2H2O.
(2)步骤②调节溶液pH选用的最佳试剂是B
A.Fe2O3 B.CuO C.Al2O3 D.NH3•H2O
(3)有关氢氧化物开始沉淀和完全沉淀的pH如表:
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 |
| 完全沉淀的pH | 5.2 | 3.7 | 9.7 | 6.7 |
(4)滤液B通过蒸发浓缩(设体积浓缩为原来的一半)、冷却结晶可以得到CuSO4•5H2O晶体.某同学认为上述操作会拌有硫酸铝晶体的析出.请你结合相关数据对该同学的观点予以评价(已知常温下,Al2(SO4)3饱和溶液中c(Al3+)=2.25mol•L-1,Ksp[Al(OH)3]=3.2×10-34)该同学的观点是错误的;通过计算可知,滤液B中,c(Al3+)=3.2×10-4mol/L,浓缩后c(Al3+)=6.4×10-4mol/L<<2.25mol/L,所以不会有硫酸铝晶体析出.
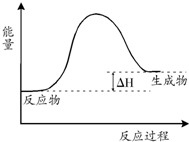
| A. | 该反应是吸热反应 | |
| B. | 当反应达到平衡时,升高温度,混合气体的颜色变浅 | |
| C. | 反应体系中加入催化剂对反应热是有影响 | |
| D. | 在反应体系中加入催化剂,正反应速率增大,逆反应速率减小 |
| A. | 64 g | B. | 32 g | C. | 1.5mol | D. | 3 mol |