题目内容
14. 元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中T单质和H2在光照的条件下发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中T单质和H2在光照的条件下发生爆炸.则下列判断正确的是( )| A. | 最简单氢化物的稳定性:R>Q>X;R>T>X | |
| B. | 五种元素中Z的活动性最弱,T的氧化物对应水化合物酸性最强 | |
| C. | Q单质能从溶液中置换出X单质,R单质能从溶液中置换出T单质 | |
| D. | X阴离子和T阴离子相比,半径:X阴离子的大;还原性:T阴离子的强 |
分析 T单质和H2在光照的条件下发生爆炸,则T为Cl元素,可推知R为F元素、X为S元素、Z为Ar、Q为O元素,结合元素周期律与元素化合物性质解答.
解答 解:T单质和H2在光照的条件下发生爆炸,则T为Cl元素,可推知R为F元素、X为S元素、Z为Ar、Q为O元素,
A.非金属性氢:R>Q>X;R>T>X,则氢化物的稳定性:R>Q>X;R>T>X,故A正确;
B.Z为Ar,原子最外层为稳定结构,活动性最弱,T为Cl元素,其最高价氧化物对应水化合物高氯酸是最强的酸,不是最高价含氧酸,则不一定,如次氯酸是弱酸,故B错误;
C.氧气与硫化氢溶液反应可以得到硫,氟气通入溶液中,与水反应生成HF与氧气,不能置换处于氯气,故C错误;
D.X阴离子和T阴离子电子层结构相同,T原子核电荷数降低,故X阴离子半径大;非金属性T较强,故T阴离子还原性较弱,故D错误;
故选A.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,A为易错点,学生容易忽略最高价氧化物,注意C选项中氟气与水,难度中等,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
4.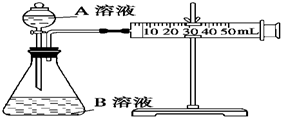 甲、乙、丙三个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.设计实验方案如下(实验中所用KMnO4溶液均已加入H2SO4):
甲、乙、丙三个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.设计实验方案如下(实验中所用KMnO4溶液均已加入H2SO4):
甲组:通过测定生成CO2气体体积的方法来比较化学反应速率的大小.
实验装置如图,实验时分液漏斗中A溶液一次性放下.
A、B的成分见下表:
(1)甲组同学实验探究的是浓度对化学反应速率的影响.
结合装置,分析所给实验仪器,定量比较①②组化学反应速率大小实现该实验目的还欠缺的仪器:秒表.
乙组通过测定单位时间内KMnO4溶液浓度变化来判定反应速率快慢.所用的试剂以及条件如下表所示:
(2)①乙组同学实验目的是探究对化学反应速率的影响.
②写出溶液中发生的反应的离子方程式(提示:H2C2O4为弱酸,KMnO4的还原产物为Mn2+):2MnO4-+5H2C2O4+6H+=2Mn2++l0CO2↑+8H2O.实验中该组同学始终没有看到溶液褪色,其原因是高锰酸钾过量.
丙组:丙组通过测定单位时间KMnO4溶液浓度变化来判定反应速率快慢.在25℃时,40mL 0.001mol/LKMnO4与38mL0.1mol/LH2C2O4和2mL2.38mol/LH2SO4混合液共80mL中KMnO4的浓度及对应时段的平均反应速率数据:
(3)完成上表中a=0.11 mol/(L•min).
问题讨论:已知该实验过程中溶液温度几乎不变,但是依据实验数据发现开始阶段速率却在增大.
你认为引起该反应速率增大的因素是反应过程中产生了催化剂加快了反应速率.
 甲、乙、丙三个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.设计实验方案如下(实验中所用KMnO4溶液均已加入H2SO4):
甲、乙、丙三个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.设计实验方案如下(实验中所用KMnO4溶液均已加入H2SO4):甲组:通过测定生成CO2气体体积的方法来比较化学反应速率的大小.
实验装置如图,实验时分液漏斗中A溶液一次性放下.
A、B的成分见下表:
| 序号 | A溶液 | B溶液 |
| ① | 2mL0.1mol/LH2C2O4溶液 | 4mL 0.01mol/L KMnO4溶液 |
| ② | 2mL0.2mol/LH2C2O4溶液 | 4mL 0.01mol/L KMnO4溶液 |
结合装置,分析所给实验仪器,定量比较①②组化学反应速率大小实现该实验目的还欠缺的仪器:秒表.
乙组通过测定单位时间内KMnO4溶液浓度变化来判定反应速率快慢.所用的试剂以及条件如下表所示:
| 序号 | 溶液 | 条件 |
| ③ | 2mL 0.1mol/L H2C2O4和8mL 0.1mol/L KMnO4 | 热水 |
| ④ | 2mL 0.1mol/L H2C2O4和8mL 0.1mol/L KMnO4 | 冷水 |
②写出溶液中发生的反应的离子方程式(提示:H2C2O4为弱酸,KMnO4的还原产物为Mn2+):2MnO4-+5H2C2O4+6H+=2Mn2++l0CO2↑+8H2O.实验中该组同学始终没有看到溶液褪色,其原因是高锰酸钾过量.
丙组:丙组通过测定单位时间KMnO4溶液浓度变化来判定反应速率快慢.在25℃时,40mL 0.001mol/LKMnO4与38mL0.1mol/LH2C2O4和2mL2.38mol/LH2SO4混合液共80mL中KMnO4的浓度及对应时段的平均反应速率数据:
| 时间(min) | 0-4 | 4-8 | 8-12 | 12-16 | 16-21 | 21-22 | 22-23 |
| c(KMnO4)(10-4mol/L) | 4.58 | 4.02 | 3.36 | 2.25 | 0.72 | 0.43 | 0.23 |
| υ(KMnO4)(10-4mol/(L•min) | a | 0.14 | 0.17 | 0.28 | 0.32 | 0.29 | 0.20 |
问题讨论:已知该实验过程中溶液温度几乎不变,但是依据实验数据发现开始阶段速率却在增大.
你认为引起该反应速率增大的因素是反应过程中产生了催化剂加快了反应速率.
5.下列反应中,一定有白色沉淀生成的是( )
①向久置的Na2SO3溶液中加入BaCl2溶液,再加入稀盐酸;
②向Na2CO3溶液中加入酸性CaCl2溶液;
③向Na2SO3溶液中通入Cl2,再滴加BaCl2和稀盐酸;
④向Na2SO3溶液中加入稀HNO3后再加入BaCl2溶液.
①向久置的Na2SO3溶液中加入BaCl2溶液,再加入稀盐酸;
②向Na2CO3溶液中加入酸性CaCl2溶液;
③向Na2SO3溶液中通入Cl2,再滴加BaCl2和稀盐酸;
④向Na2SO3溶液中加入稀HNO3后再加入BaCl2溶液.
| A. | ①②④ | B. | ①②③ | C. | ①③④ | D. | ②③④ |
2.下列反应过程中的能量变化情况符合图的是( )


| A. | Ba(OH)2•8H2O与NH4C1反应 | B. | 氢气在氯气中燃烧 | ||
| C. | 镁和盐酸的反应 | D. | 钠和水反应 |
9.下列说法中正确的是( )
| A. | 在常温常压下,“氢化油”呈液态 | |
| B. | 纤维素和淀粉均属于“糖类,它们在人体内水解的最终产物均为葡萄糖 | |
| C. | 要鉴别石蜡油中是否混有少量苯,可加入四氯化碳,萃取,观察是否分层 | |
| D. | 用灼烧闻气味的方法来区别棉织物和毛织物 |
19.NA表示阿伏加德罗常数的值,下列说正确的( )
| A. | 17g氨气中所含质子数为10NA | |
| B. | 2.4g金属镁变成镁离子时失去电子数为0.1NA | |
| C. | 在标准状况下,22.4L氧气中所含的氧原子数为NA | |
| D. | 在25℃、压强为1.01×105Pa时,28g氮气所含的分子数为NA |
6.实验室区别乙烷和乙烯不可采用的方法是( )
| A. | 分别通入酸性KMnO4溶液中 | B. | 分别点燃观察火焰 | ||
| C. | 分别通入澄清石灰水中 | D. | 分别通入溴水中 |
2.给定条件下,下列选项中所示的物质间转化均不能一步实现的是( )
| A. | 粗硅$→_{高温}^{Cl_{2}}$SiCl4$→_{高温}^{H_{2}}$Si | |
| B. | Mg(OH)2$\stackrel{盐酸}{→}$MgCl2 $\stackrel{电解}{→}$Mg | |
| C. | Na$→_{△}^{O_{2}}$Na2O2$\stackrel{H_{2}O}{→}$NaOH | |
| D. | AgNO3(aq)$\stackrel{NH_{3}•H_{2}O}{→}$[Ag(NH3)2]OH(aq)$\stackrel{蔗糖△}{→}$Ag |
3.不能正确表示原子轨道的是( )
| A. | 2s | B. | 5f | C. | 2d | D. | 3px |